题目内容
常温下,某溶液中水电离出的c(OH-)>1×10-7mol?L-1,则该溶液不可能的构成是( )
| A、OH-、Br-、SO42-、K+ |
| B、F-、Na+、K+、NO3- |
| C、Na+、NH4+、CH3COO-、SO42- |
| D、K+、NO3-、NH4+、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:常温下,某溶液中水电离出的c(OH-)>1×10-7mol?L-1,促进水的电离,为盐的水解,溶液可能呈酸性也可能呈碱性,溶液所构成离子,应能大量共存,离子之间不发生任何反应,结合对应离子的性质解答该题.
解答:
解:A.如溶液呈碱性,离子之间不发生任何反应,可大量共存,故A不选;
B.如溶液呈碱性,离子之间不发生任何反应,可大量共存,故B不选;
C.CH3COO-在酸性条件下不能大量共存,NH4+在碱性条件下不能大量共存,故C选;
D.酸性条件下,离子之间不发生任何反应,可大量共存,故D不选.
故选C.
B.如溶液呈碱性,离子之间不发生任何反应,可大量共存,故B不选;
C.CH3COO-在酸性条件下不能大量共存,NH4+在碱性条件下不能大量共存,故C选;
D.酸性条件下,离子之间不发生任何反应,可大量共存,故D不选.
故选C.
点评:本题考查离子共存问题,为高频考点,侧重于学生的分析能力的考查,注意把握离子的性质以及反应类型的判断,本题注意溶液酸碱性的判断,为解答该题的关键,难度不大.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
下列反应原理不符合工业冶炼金属实际情况的是( )
A、2HgO
| ||||
B、2NaCl(熔融)
| ||||
C、2MgO(熔融)
| ||||
D、Fe2O3+3CO
|
最近科学家成功制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是( )
| A、该晶体类型是原子晶体 |
| B、该晶体中碳原子和氧原子的个数比为1:2 |
| C、每摩尔该晶体中含4molC-O |
| D、晶体的空间最小环共有6个原子构成 |
下列叙述正确的是( )
| A、1.00molNaCl中含有6.02×1023个NaCl分子 |
| B、欲配置1.00L1.00mol/L的NaCl溶液,可将58.5gNaCl溶于1.00L水中 |
| C、1molNO2和N2O4混合气体中含有原子总数为3NA |
| D、1molNa与足量的O2反应,生成Na2O和Na2O2的混合物,共转移NA个电子 |
下列各组物质中,互为同系物的是( )
A、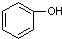 与 与 |
B、 与 与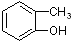 |
| C、CH3Cl与CH2Cl2 |
| D、甲醇与乙二醇 |
下列事实不能用勒夏特列原理来解释的是( )
| A、加压有利于SO2与O2反应生成SO3 |
| B、用过量空气煅烧硫铁矿可以提高原料的利用率 |
| C、加入催化剂都能使合成氨的反应速率加快 |
| D、温度过高对合成氨反应不利 |
我国镍氢电池居世界先进水平,我军潜艇将装备国产大功率镍氢动力电池.常见镍氢电池的某极是储氢合金LaNi5H6 (LaNi5H6中各元素化合价均为零),电池反应通常表示为:LaNi5H6+6NiO(OH)
LaNi5+6Ni(OH)2,下列说法正确的是( )
| 放电 |
| 充电 |
| A、充电时储氢合金作阳极 |
| B、放电时每转移6mol电子,有6mol NiO(OH)被氧化 |
| C、充电时阳极周围PH增大 |
| D、放电时负极反应:LaNi5H6+6OH--6e-═LaNi5+6H2O |
下列有机物命名正确的是( )
| A、H2N-CH2COOH 氨基乙酸 |
B、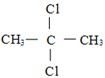 2-二氯丙烷 2-二氯丙烷 |
C、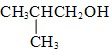 2-甲基丙醇 2-甲基丙醇 |
| D、C17H33COOH 硬脂酸 |