胶体区别于其它分散系最本质的特征是( )
| A、外观澄清、稳定 |
| B、丁达尔现象 |
| C、分散至粒子能透过半透膜 |
| D、分散质粒子直径为1---100nm |
某同学设计如图所示装置,探究氯碱工业原理,下列说法正确的是( )
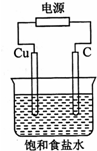

| A、石墨电极与直流电源负极相连 |
| B、用湿润KI淀粉试剂在铜电极附近检验气体,试纸变蓝色 |
| C、氢氧化钠在石墨电极附近产生,Na+向石墨电极迁移 |
| D、铜电极的反应式为:2H++2e-═H2↑ |
能正确表示下列反应的离子方程式的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、电解饱和食盐水:2Cl-+H2O═2OH-+H2↑+Cl2↑ |
| C、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| D、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
见光能分解的盐是( )
| A、HClO |
| B、AgBr |
| C、氯水 |
| D、Ca(ClO)2 |
FeCl3、CuCl2的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
| A、剩余固体中一定含Cu |
| B、溶液中一定含Cu2+ |
| C、加入KSCN溶液一定不变红色 |
| D、溶液中一定含Fe2+ |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、1.8g的NH4+离子中含有的电子数为0.1NA | ||
| B、常温常压下,48gO3和O2的混合物含有的氧原子数为3NA | ||
| C、11.2L氧气中所含有的氧原子数为NA | ||
D、标准状况下,1L水所含分子数为
|
电解一定量的硫酸铜溶液的实验装置如图①,电解的实验数据如图②,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法正确的是( )
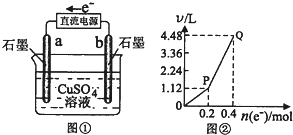

| A、开始时b电极有红色物质析出,而后有气泡产生 |
| B、a电极上的电子经溶液流向b极再流入直流电源 |
| C、曲线P~Q段表示产生H2和O2的体积比为1:2 |
| D、从开始到Q点收集到的混合气体中有0.1mol氧气 |
某温度下,反应SO2(g)+
O2(g)?SO3 (g) 的平衡常数K1=100,在同一温度下,反应2SO3(g)?2SO2(g)+O2(g)的平衡常数K2的值为( )
| 1 |
| 2 |
| A、104 |
| B、200 |
| C、10-4 |
| D、10-2 |
溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )
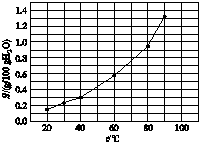

| A、60℃时溴酸银的Ksp约等于6×10-4 |
| B、温度升高时溴酸银溶解速度加快 |
| C、溴酸银的溶解时放热过程 |
| D、若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 |
下列有关实验装置的说法中正确的是( )
A、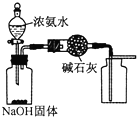 可制取干燥纯净的NH3 |
B、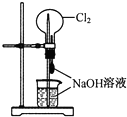 可以完成“喷泉”实验 |
C、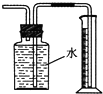 可测量Cu 与浓硝酸反应产生气体的体积 |
D、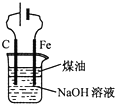 可用于实验室制备Fe (OH)2 |