题目内容
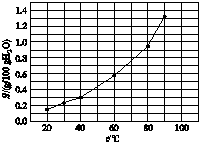
溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )

| A、60℃时溴酸银的Ksp约等于6×10-4 |
| B、温度升高时溴酸银溶解速度加快 |
| C、溴酸银的溶解时放热过程 |
| D、若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 |
考点:溶解度、饱和溶液的概念
专题:物质的量浓度和溶解度专题
分析:A.60℃溴酸银的溶解度大约是0.6g.则c(AgBrO3)=
=0.025mol/L,Ksp=c(Ag+)?c(BrO3-)=0.025×0.025≈6×10-4;
B.温度升高,溴酸银溶解在水中的微粒运动速度加快,扩散的更快,故溶解速度加快;
C.无法判断其溶解过程的热效应;
D.由于硝酸钾的溶解度随温度变化比较大,而溴酸银的溶解度随温度变化不大.
| ||
| 0.1 |
B.温度升高,溴酸银溶解在水中的微粒运动速度加快,扩散的更快,故溶解速度加快;
C.无法判断其溶解过程的热效应;
D.由于硝酸钾的溶解度随温度变化比较大,而溴酸银的溶解度随温度变化不大.
解答:
解:A.60℃溴酸银的溶解度大约是0.6g.则c(AgBrO3)=
=0.025mol/L,Ksp=c(Ag+)?c(BrO3-)=0.025×0.025≈6×10-4,故A正确;
B.温度升高,溴酸银溶解在水中的微粒运动速度加快,扩散的更快,故溶解速度加快,故B正确;
C.该图象只是给出溴酸银的溶解度与温度的关系,无法判断其溶解过程的热效应,故C错误;
D.由于硝酸钾的溶解度随温度变化比较大,而溴酸银的溶解度随温度变化不大,所以若硝酸钾中含有少量溴酸银,可用重结晶方法提纯,故D正确;
故选C.
| ||
| 0.1 |
B.温度升高,溴酸银溶解在水中的微粒运动速度加快,扩散的更快,故溶解速度加快,故B正确;
C.该图象只是给出溴酸银的溶解度与温度的关系,无法判断其溶解过程的热效应,故C错误;
D.由于硝酸钾的溶解度随温度变化比较大,而溴酸银的溶解度随温度变化不大,所以若硝酸钾中含有少量溴酸银,可用重结晶方法提纯,故D正确;
故选C.
点评:本题考查溶解度的概念及相关计算,难度中等.要注意重结晶方法的使用对象.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
 X、Y、Z、W四种短周期元素在周期表中的位置如图所示.已知这四种元素原子的核电荷数之和为36.则这四种元素按X、Y、Z、W顺序依次是( )
X、Y、Z、W四种短周期元素在周期表中的位置如图所示.已知这四种元素原子的核电荷数之和为36.则这四种元素按X、Y、Z、W顺序依次是( )| A、N、P、O、C |
| B、C、N、O、P |
| C、O、S、N、F |
| D、C、Si、Al、N |
将过量的SO2气体通入下列溶液中,最终没有沉淀的是( )
| A、Na[Al(OH)4] |
| B、BaCl2 |
| C、Ba(NO3)2 |
| D、Na2SiO3 |
下列反应属于放热反应的是( )
A、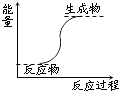 能量变化如图所示的反应 |
| B、燃烧反应和铝热反应 |
| C、化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
| D、氢氧化钡晶体和氯化铵晶体的反应 |
用化学方法区别SO2与CO2最好选用的化学试剂是( )
| A、紫色的石蕊试液 |
| B、品红溶液 |
| C、澄清的石灰水 |
| D、氢氧化钠溶液 |
见光能分解的盐是( )
| A、HClO |
| B、AgBr |
| C、氯水 |
| D、Ca(ClO)2 |
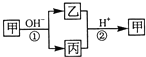 甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )| A、X元素可能为Al |
| B、X 元素不一定为非金属元素 |
| C、反应①和②互为可逆反应 |
| D、反应①和②一定为氧化还原反应 |
下列各组中的两种物质相互作用时,改变反应条件或反应物的用量,不会影响产物组成的是( )
| A、Na与O2 |
| B、NaOH与CO2 |
| C、NaOH与AlCl3 |
| D、Na2O与CO2 |
 一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )
一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )