题目内容
FeCl3、CuCl2的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
| A、剩余固体中一定含Cu |
| B、溶液中一定含Cu2+ |
| C、加入KSCN溶液一定不变红色 |
| D、溶液中一定含Fe2+ |
考点:铁盐和亚铁盐的相互转变,铜金属及其重要化合物的主要性质
专题:元素及其化合物
分析:根据三价铁离子、铜离子的氧化性强弱判断反应先后顺序,从而确定固体的成分、溶液的成分;有固体剩余,若固体只有铜,则反应后的溶液中一定无三价铁离子存在,一定存在亚铁离子,可能含有铜离子;若有铁剩余,一定有铜生成,三价铁离子和铜离子无剩余,据此进行判断.
解答:
解:①当固体为铁、铜时,溶液中的Fe3+、Cu2+全部参加反应生成Fe2+和Cu,反应的方程式为:2FeCl3+Fe=3FeCl2、CuCl2+Fe=Cu+FeCl2,所以溶液中一定没有Fe3+、Cu2+,一定含有Fe2+;
②当固体为铜时,溶液中一定没有Fe3+,Cu2+恰好全部参加反应或部分反应生成Fe2+和Cu,所以溶液中一定没有Fe3+,可能含有Cu2+,一定含有Fe2+;
A、通过以上分析知,剩余固体中一定含Cu,故A正确;
B、通过以上分析知,溶液中可能含有Cu2+,故B错误;
C、溶液中一定不含Fe3+,所以加入KSCN溶液不变红色,故C正确;
D、通过以上分析知,溶液中一定含有Fe2+,故D正确;
故选B.
②当固体为铜时,溶液中一定没有Fe3+,Cu2+恰好全部参加反应或部分反应生成Fe2+和Cu,所以溶液中一定没有Fe3+,可能含有Cu2+,一定含有Fe2+;
A、通过以上分析知,剩余固体中一定含Cu,故A正确;
B、通过以上分析知,溶液中可能含有Cu2+,故B错误;
C、溶液中一定不含Fe3+,所以加入KSCN溶液不变红色,故C正确;
D、通过以上分析知,溶液中一定含有Fe2+,故D正确;
故选B.
点评:本题考查了Fe3+、Cu2+的氧化能力大小的比较,能正确判断固体的成分是解本题的关键,根据固体的成分了解反应的先后顺序,从而确定溶液的成分.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
下列现象或事实可用同一原理解释的是( )
| A、浓硫酸和浓盐酸长期暴露在空气中浓度降低 |
| B、SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色,其原理相同 |
| C、水玻璃和Na2SO3长期暴露在空气中变质 |
| D、常温下铁分别加入浓硫酸和浓硝酸中均无明显现象 |
某混合气体中可能含有H2、CO、CO2、HCl、NH3及水蒸气中的两种或多种.当混合气体依次通过足量下列物质时会发生括号中所说明的现象:
①澄清的石灰水(无浑浊);
②氢氧化钡溶液(有混浊现象);
③浓硫酸(无明显现象);
④灼热的氧化铜(变红);
⑤无水硫酸铜(变蓝).
下列对该混合气体成分的判断正确的是( )
①澄清的石灰水(无浑浊);
②氢氧化钡溶液(有混浊现象);
③浓硫酸(无明显现象);
④灼热的氧化铜(变红);
⑤无水硫酸铜(变蓝).
下列对该混合气体成分的判断正确的是( )
| A、一定没有CO2、肯定有CO和H2 |
| B、一定有CO2、CO和水蒸气 |
| C、一定有H2、HCl和CO2、可能含有CO |
| D、可能有CO2、NH3和水蒸气 |
下列各组溶液中,只用试管和胶头滴管,不用其他任何试剂就能鉴别的是( )
| A、AlCl3和NaOH |
| B、KCl和NaCl |
| C、NaCl和AgNO3 |
| D、Na2CO3和Ba(OH)2 |
下列有关实验装置的说法中正确的是( )
A、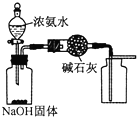 可制取干燥纯净的NH3 |
B、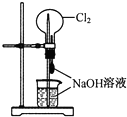 可以完成“喷泉”实验 |
C、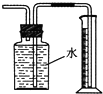 可测量Cu 与浓硝酸反应产生气体的体积 |
D、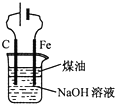 可用于实验室制备Fe (OH)2 |
下列离子组能大量共存的是( )
| A、Ba2+、Cl-、SO42-、K+ |
| B、Mg2+、SO42-、Na+、Cl- |
| C、H+、CO32-、Al3+、Cl- |
| D、K+、Fe2+、NO3-、H+ |
下列有关说法中正确的是( )
| A、从组成元素上可以区别纯净物和混合物 |
| B、往Fe(OH)3胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解 |
| C、通过化学变化可以实现16O与18O问的相互转化 |
| D、鸡蛋清溶液中加入饱和(NH4)2SO4溶液生成白色沉淀,属于化学变化 |
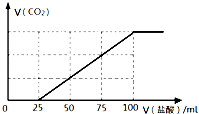 向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )
向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )| A、原NaOH溶液的浓度为0.2 mol/L |
| B、通入CO2的体积为448 mL |
| C、所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=1:3 |
| D、所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=1:1 |