题目内容
能正确表示下列反应的离子方程式的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、电解饱和食盐水:2Cl-+H2O═2OH-+H2↑+Cl2↑ |
| C、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| D、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成碳酸钙和次氯酸;
B.电解饱和食盐水时条件是电解;
C.二者反应生成碳酸钙、氢氧化钠和水;
D.酸性条件下不能生成氢氧根离子.
B.电解饱和食盐水时条件是电解;
C.二者反应生成碳酸钙、氢氧化钠和水;
D.酸性条件下不能生成氢氧根离子.
解答:
解:A.二者反应生成碳酸钙和次氯酸,离子方程式为2ClO-+CO2+H2O+Ca2+═2HClO+CaCO3↓,故A错误;
B.电解饱和食盐水时条件是电解,离子方程式为2Cl-+H2O
2OH-+H2↑+Cl2↑,故B错误;
C.二者反应生成碳酸钙、氢氧化钠和水,离子方程式为Ca2++OH-+HCO3-═CaCO3↓+H2O,故C正确;
D.酸性条件下不能生成氢氧根离子,离子方程式为5I-+IO3-+6H+═3I2+H2O,故D错误;
故选C.
B.电解饱和食盐水时条件是电解,离子方程式为2Cl-+H2O
| ||
C.二者反应生成碳酸钙、氢氧化钠和水,离子方程式为Ca2++OH-+HCO3-═CaCO3↓+H2O,故C正确;
D.酸性条件下不能生成氢氧根离子,离子方程式为5I-+IO3-+6H+═3I2+H2O,故D错误;
故选C.
点评:本题考查离子方程式正误判断,明确物质的性质及离子方程式书写规则即可解答,注意不能漏掉某些离子反应,要遵循电荷守恒、原子守恒及转移电子守恒,不能漏写反应条件,易错选项是D.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列实验能获得成功的是( )
| A、苯和浓溴水用FeBr3作催化剂制溴苯 |
| B、氯乙烷与NaOH溶液共热,在水解后的溶液中加入AgNO3溶液检验Cl- |
| C、乙烯通入含Br2的CCl4溶液制得CH2BrCH2Br |
| D、将无水乙醇加热到170℃制取乙烯 |
正确掌握化学用语是学好化学的基础.下列化学用语中不正确的是( )
| A、乙烯的结构简式CH2=CH2 |
B、CH4分子的球棍模型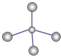 |
C、Ca2+的结构示意图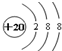 |
| D、乙醇的分子式 C2H6O |
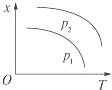 如图表示温度和压强对平衡状态下可逆反应2M(g)+N(g)?2Q(g)△H<0的影响.下列有关说法正确的是( )
如图表示温度和压强对平衡状态下可逆反应2M(g)+N(g)?2Q(g)△H<0的影响.下列有关说法正确的是( )| A、x不可能是M或N的体积分数 |
| B、x可能是混合气体的物质的量 |
| C、该反应在p1时先达到化学平衡状态 |
| D、p1>p2 |
某温度下,反应SO2(g)+
O2(g)?SO3 (g) 的平衡常数K1=100,在同一温度下,反应2SO3(g)?2SO2(g)+O2(g)的平衡常数K2的值为( )
| 1 |
| 2 |
| A、104 |
| B、200 |
| C、10-4 |
| D、10-2 |
下列溶液中Cl-的物质的量与5L1mol?L-1 AlCl3溶液中Cl-的物质的量相等的是( )
| A、1.5L1mol?L-1的NaCl溶液 |
| B、7.5L2mol?L-1NH4Cl溶液 |
| C、15L2mol?L-1的KCl溶液 |
| D、7.5L1mol?L-1的FeCl3溶液 |
下列溶液中不能通过化学反应区别SO2和CO2气体的是( )
| A、澄清石灰水 |
| B、KMnO4酸性溶液 |
| C、氯水 |
| D、品红溶液 |
下列说法正确的是( )
| A、H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体;甲醇、乙二醇和丙三醇互为同系物 |
| B、在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C、HI的相对分子质量大于HF,所以HI的沸点高于HF |
| D、由IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子型化合物 |
 科学研究发现Cu2O可作为太阳光分解水的催化剂.
科学研究发现Cu2O可作为太阳光分解水的催化剂.