题目内容
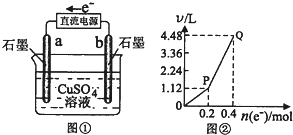
电解一定量的硫酸铜溶液的实验装置如图①,电解的实验数据如图②,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法正确的是( )

| A、开始时b电极有红色物质析出,而后有气泡产生 |
| B、a电极上的电子经溶液流向b极再流入直流电源 |
| C、曲线P~Q段表示产生H2和O2的体积比为1:2 |
| D、从开始到Q点收集到的混合气体中有0.1mol氧气 |
考点:电解原理
专题:电化学专题
分析:根据电子流向知,a为阴极、b为阳极,开始时,阴极上铜离子放电、阳极上氢氧根离子放电,所以电池反应式为2Cu2++2H2O
2Cu+O2↑+4H+,当铜离子完全放电后,再继续电解相当于电解水,电池反应式为2H2O
2H2↑+O2↑,所以从O到P点,生成的气体为氧气,从P到Q点生成的气体是氧气和氢气,
P点收集到n(O2)=
=0.05mol,从P到Q收集到气体体积=4.48L-1.12L=3.36L,其物质的量=
=0.15mol,根据2H2O
2H2↑+O2↑,从P到Q收集的氢气和氧气物质的量之比为2:1,则从P到Q点收集到的氢气物质的量是0.1mol、氧气的物质的量是0.05mol,据此分析解答.
| ||
| ||
P点收集到n(O2)=
| 1.12L |
| 22.4L/mol |
| 3.36L |
| 22.4L/mol |
| ||
解答:
解:根据电子流向知,a为阴极、b为阳极,开始时,阴极上铜离子放电、阳极上氢氧根离子放电,所以电池反应式为2Cu2++2H2O
2Cu+O2↑+4H+,当铜离子完全放电后,再继续电解相当于电解水,电池反应式为2H2O
2H2↑+O2↑,所以从O到P点,生成的气体为氧气,从P到Q点生成的气体是氧气和氢气,
P点收集到n(O2)=
=0.05mol,从P到Q收集到气体体积=4.48L-1.12L=3.36L,其物质的量=
=0.15mol,根据2H2O
2H2↑+O2↑,从P到Q收集的氢气和氧气物质的量之比为2:1,则从P到Q点收集到的氢气物质的量是0.1mol、氧气的物质的量是0.05mol,
A.b为阳极,阳极上电极反应式为2H2O-4e-=4H++O2↑,所以b电极上只有无色气泡生成,故A错误;
B.电子不进入电解质溶液,电解质溶液中阴阳离子定向移动形成电流,故B错误;
C.曲线P~Q段实质上是电解水,所以表示产生H2和O2的体积比为2:1,故C错误;
D.从开始到Q点收集到的混合气体中氧气的物质的量=0.05mol×2=0.1mol,故D正确;
故选D.
| ||
| ||
P点收集到n(O2)=
| 1.12L |
| 22.4L/mol |
| 3.36L |
| 22.4L/mol |
| ||
A.b为阳极,阳极上电极反应式为2H2O-4e-=4H++O2↑,所以b电极上只有无色气泡生成,故A错误;
B.电子不进入电解质溶液,电解质溶液中阴阳离子定向移动形成电流,故B错误;
C.曲线P~Q段实质上是电解水,所以表示产生H2和O2的体积比为2:1,故C错误;
D.从开始到Q点收集到的混合气体中氧气的物质的量=0.05mol×2=0.1mol,故D正确;
故选D.
点评:本题考查电解原理,明确电极上离子放电顺序是解本题关键,知道图②中曲线各段发生的反应即可解答,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
要除去混在氮气中的二氧化碳和一氧化碳得到纯净、干燥的氮气,正确方法是( )
| A、先通过石灰水,在通过灼热的氧化铜 |
| B、先通过常温下的氧化铜,再通过氢氧化钠 |
| C、先通过灼热的氧化铜,再通过氢氧化钠溶液,最后通过浓硫酸 |
| D、先通过灼热的铜,再通过石灰水 |
下列药品可用带玻璃塞的试剂瓶储存的是( )
| A、稀盐酸 |
| B、氢氟酸 |
| C、NaOH溶液 |
| D、Na2SiO3溶液 |
能正确表示下列反应的离子方程式是( )
| A、明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓ |
| B、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| C、钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ |
| D、硫酸铜溶液中加入过量氨水:Cu2++2OH-═Cu(OH)2↓ |
某同学设计如图所示装置,探究氯碱工业原理,下列说法正确的是( )
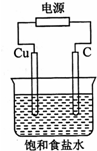

| A、石墨电极与直流电源负极相连 |
| B、用湿润KI淀粉试剂在铜电极附近检验气体,试纸变蓝色 |
| C、氢氧化钠在石墨电极附近产生,Na+向石墨电极迁移 |
| D、铜电极的反应式为:2H++2e-═H2↑ |
下列离子方程式书写正确的是( )
| A、碳酸氢钠与盐酸反应:CO32-+2H+═CO2↑+H2O |
| B、氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
| C、钠投入硫酸铜溶液中:2Na+Cu2+═2Na++Cu |
| D、碳酸氢钠溶液中加入烧碱溶液:HCO3-+OH-═CO32-+H2O |
下列有关除杂的操作不正确的是( )
| A、铁粉中混有少量铝粉:加入过量烧碱溶液,过滤 |
| B、碳酸氢钠粉末中含有少量碳酸钠粉末:加热 |
| C、除去FeCl3溶液中的FeCl2:加入氯水 |
| D、FeCl3药品中混有少量AlCl3:溶解、加入过量NaOH溶液过滤、将沉淀溶于盐酸 |