Se是人体必需微量元素,下列有关
Se和
Se的说法正确的是( )
78 34 |
80 34 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A、将0.2 mol?L-1 CH3COOH溶液和0.1 mol?L-1 NaOH溶液等体积混合,则反应后的混合液中:2c(OH-)+c(CH3COO-)=2c(H+)+c(CH3COOH) | ||||
B、物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中,c(N
| ||||
C、0.1 mol?L-1 NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(HC
| ||||
D、一定量(NH4)2SO4与NH3?H2O混合所得的酸性溶液中:c(N
|
 夜色中常看到小朋友手持被称为“魔棒”的荧光棒玩耍,“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式为:下列有关说法不正确的是( )
夜色中常看到小朋友手持被称为“魔棒”的荧光棒玩耍,“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式为:下列有关说法不正确的是( )| A、草酸二酯属于芳香族化合物 |
| B、草酸二酯的分子式为C26H24O8Cl6 |
| C、草酸二酯是高分子化合物 |
| D、草酸二酯苯环上氢原子被一个溴原子取代的产物只有一种 |
把过量的CO2气体通入下列物质的饱和溶液中,不变浑浊的是( )
| A、Ca(OH)2 |
| B、C6H5ONa |
| C、NaAlO2 |
| D、Na2SiO3 |
| E、Na2CO3 |
| F、CaCl2 |
已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI+13I2+12K2SO4+12H2O下列说法正确的是( )
| A、CuI是氧化剂 |
| B、2mol氧化剂在反应中得到的电子为10 mol |
| C、24mol KI在反应中失去的电子为22mol |
| D、氧化剂与还原剂的物质的量之比为1:12 |
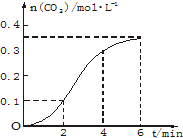 CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图.下列结论正确的是( )
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图.下列结论正确的是( )| A、反应开始4 min内温度对反应速率的影响比浓度小 |
| B、反应4 min后平均反应速率最小 |
| C、反应开始2 min内平均反应速率最大 |
| D、反应在第2 min到第4 min间生成CO2的平均反应速率为 v(CO2)=0.1 mo1?(L?min)-1 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、含有相同氧原子数的SO2和CO的质量相等 |
| B、2g氢气所含原子数目为NA |
| C、lmol氨气含有的原子数目为2NA |
| D、l7g氨气所含电子数目为l0NA |
将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述中不正确的是( )
| A、该分散系不能发生丁达尔现象 |
| B、该分散质颗粒能透过滤纸 |
| C、该分散质颗粒能透过半透膜 |
| D、该分散质颗粒能发生布朗运动 |
下列各组混合物中,不能通过分液进行分离的是( )
| A、溴乙烷和水 | B、甲苯和水 |
| C、乙醛和乙醇 | D、乙醛和水 |
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法不正确的是( )

| A、由精盐制备NaHCO3的反应本质上属于复分解反应 |
| B、用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C、氯碱工业是通过电解饱和食盐水得到烧碱、氯气和氢气;工业上制取金属镁是通过电解饱和MgCl2溶液 |
| D、在第④步反应中Br2既是氧化剂又是还原剂,在第⑤步反应中Br2既是氧化产物又是还原产物 |