题目内容
Se是人体必需微量元素,下列有关
Se和
Se的说法正确的是( )
78 34 |
80 34 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
考点:核素,同位素及其应用,同素异形体
专题:原子组成与结构专题
分析:根据质子数、中子数、质量数的关系判断A、B,根据定义判断C、D.
解答:
解:A.Se的两种同位素的质子数都为34,故A错误;
B.3478Se和3480Se的中子数分别为44和46,故B错误;
C.3478Se和3480Se是原子,属同位素,故C正确;
D.同素异形体指单质而同位素指原子,故D错误.
故选C.
B.3478Se和3480Se的中子数分别为44和46,故B错误;
C.3478Se和3480Se是原子,属同位素,故C正确;
D.同素异形体指单质而同位素指原子,故D错误.
故选C.
点评:本题考查原子结构的有关“粒子数”的关系及同位素、同素异形体的概念,侧重考查学生的辨别能力,难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
| A、向水中加人稀醋酸,平衡逆向移动,c(OH-)降低 |
| B、向水中加入少量固体碳酸氢钠,c(H+)增大,Kw不变 |
| C、向水中加人少量固体CH3COONa,能促进水的电离 |
| D、压强增大,平衡向逆反应方向移动 |
a、b、c、d四个集气瓶中装有Cl2、H2、HCl、HBr中的一种气体,若a、d两瓶气体混合见光爆炸,a、b两瓶气体混合瓶壁出现暗红色小液滴,则c瓶装的气体是( )
| A、HBr |
| B、HCl |
| C、Cl2 |
| D、H2 |
某无色混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种.现将此无色混合气体通过品红溶液,品红溶液退色,把剩余气体排入空气中,很快变为红棕色.下列对原混合气体成分的判断,正确的是( )
| A、肯定有SO2和NO |
| B、肯定有Cl2、O2和NO2 |
| C、可能有Cl2和O2 |
| D、肯定只有NO |
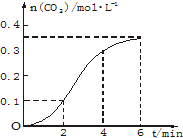 CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图.下列结论正确的是( )
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图.下列结论正确的是( )| A、反应开始4 min内温度对反应速率的影响比浓度小 |
| B、反应4 min后平均反应速率最小 |
| C、反应开始2 min内平均反应速率最大 |
| D、反应在第2 min到第4 min间生成CO2的平均反应速率为 v(CO2)=0.1 mo1?(L?min)-1 |
下列各组中的两种相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是( )
①碳酸钠溶液与盐酸
②偏铝酸钠溶液与盐酸
③二氧化碳与烧碱溶液
④碳酸氢钠与澄清石灰水
⑤氯化铝与氨水.
①碳酸钠溶液与盐酸
②偏铝酸钠溶液与盐酸
③二氧化碳与烧碱溶液
④碳酸氢钠与澄清石灰水
⑤氯化铝与氨水.
| A、③⑤ | B、①③④ | C、仅有⑤ | D、② |
观察是研究物质性质的一种基本方法.某同学将一小块金属钠露置于空气中,观察到下列现象:银白色
变灰暗
变白色
出现液滴
白色固体,则下列说法正确的是( )
| ① |
| ② |
| ③ |
| ④ |
| A、①发生氧化还原反应生成了过氧化钠 |
| B、④只发生物理变化 |
| C、③是碳酸钠吸收空气中的水蒸气形成了溶液 |
| D、②变白色主要是因为生成了氢氧化钠 |
在密闭容器中,有可逆反应:nA(气)+mB(气)?pC(气)△H=Q处于平衡状态(已知m+n>p,Q>0)下列说法中正确的是( )
①升高温度时,[B]/[C]的值减小;②降温时,体系内混合气体的平均摩尔质量减小;③加入B后,A的转化率变大;④加入催化剂,气体总物质的量不变;⑤充入C后,A,B的物质的量增大.
①升高温度时,[B]/[C]的值减小;②降温时,体系内混合气体的平均摩尔质量减小;③加入B后,A的转化率变大;④加入催化剂,气体总物质的量不变;⑤充入C后,A,B的物质的量增大.
| A、③④ | B、②③⑤ |
| C、①②⑤ | D、全部 |
 一定温度下,将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如图中曲线a.已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是( )
一定温度下,将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如图中曲线a.已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是( )| A、将饱和氯水升温,继续通入Cl2时,溶液中c(H+)变化如曲线b |
| B、在饱和氯水中通入SO2气体,溶液中c(H+)变化如曲线b |
| C、降温,继续通入Cl2时,溶液中c(H+)增大 |
| D、在饱和氯水中加入NaOH使 pH=7,所得溶液中存在下列关系c(Na+)>c(ClO-)>c(Cl-)>c(HClO) |