NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、在常温下常压下,11.2 L氯气含有的分子数为0.5NA |
| B、在常温下常压下,1 mol氦气含有的分子数为2NA |
| C、32g氧气所含原子数目为2NA |
| D、在同温同压时,相同体积的任何气体单质所含的原子数目相同 |
25℃和101kPa时,乙烷,乙炔和丙烯组成的混合烃8mL与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了18mL,原混合烃中乙炔的体积分数为( )
| A、12.5% | B、25% |
| C、50% | D、75% |
将2.72g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得反应后放出标准状况下气体0.224L.则下列判断中正确的是( )
| A、原混合物中n(Fe):n(Fe2O3)=3:1 |
| B、反应后溶液中Fe2+和Fe3+的物质的量之比为3:1 |
| C、实际参加反应HCl的物质的量为0.08mol |
| D、向溶液中滴入KSCN溶液,显红色 |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 除去HC1中含有的少量Cl2 |
B、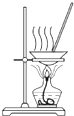 将硫酸铜溶液蒸干,制备蓝矾 |
C、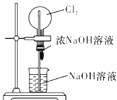 可以完成“喷泉”实验 |
D、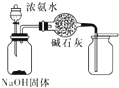 制取并收集干燥纯净的NH3 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、56 g Fe在过量的 C12中充分燃烧,转移的电子数为2NA |
| B、常温常压下,22 g 氧气和26 g 臭氧所含氧原子数之和为3 NA |
| C、标准状况下,2.24L CHCl3含有的分子数为0.1NA |
| D、常温常压下,2.8g N2所含电子数为NA |
能正确表示下列化学反应的离子方程式是( )
| A、用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O═2HCO3-+SO32- |
| B、硫酸亚铁溶液中加入过氧化氢溶液:2H2O2+Fe2++4H+═Fe3++4H2O |
| C、次氯酸钙溶液中通往过量的SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| D、碳酸镁溶液于硝酸中:MgCO3+2H+═Mg2++H2O+CO2↑ |
下面是有关氢硫酸(H2S水溶液):
①蒸馏水中通入H2S至饱和,敞口存放两天,明显失效,但无沉淀;若密闭保存一个月,既不浑浊,也不失效.
②自来水中通入H2S,出现浑浊现象,因此不能做为H2S饱和溶液使用.
根据以上事实,判断以下说法不正确的是( )
①蒸馏水中通入H2S至饱和,敞口存放两天,明显失效,但无沉淀;若密闭保存一个月,既不浑浊,也不失效.
②自来水中通入H2S,出现浑浊现象,因此不能做为H2S饱和溶液使用.
根据以上事实,判断以下说法不正确的是( )
| A、氢硫酸失效的原因是易被O2氧化 |
| B、氢硫酸失效的原因是H2S易挥发 |
| C、氢硫酸这种试剂一定要现用现制 |
| D、自来水中存在着较强的氧化性物质 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、含有NA个原子的氢气在标准状况下的体积约为22.4 L |
| B、25℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA |
| C、40 g NaOH溶解在1 L水中,所制得的100 mL溶液中含Na+数为0.1NA |
| D、标准状况下,11.2 L H2O含有的分子数为0.5NA |
化学与生产、生活、社会密切相关.下列有关说法中不正确的是( )
| A、聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 |
| B、使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾 |
| C、植物油和裂化汽油都可以使溴水褪色 |
| D、神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |