题目内容
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 除去HC1中含有的少量Cl2 |
B、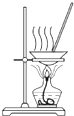 将硫酸铜溶液蒸干,制备蓝矾 |
C、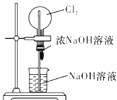 可以完成“喷泉”实验 |
D、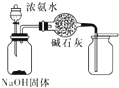 制取并收集干燥纯净的NH3 |
考点:化学实验方案的评价,气体的净化和干燥
专题:实验评价题
分析:A.氯气难溶于饱和食盐水,不能被饱和氯化钠溶液吸收;
B.应用余热蒸干;
C.氯气与NaOH溶液反应,可形成喷泉;
D.氨气密度比空气小,应用向下排空法收集.
B.应用余热蒸干;
C.氯气与NaOH溶液反应,可形成喷泉;
D.氨气密度比空气小,应用向下排空法收集.
解答:
解:A.氯气难溶于饱和食盐水,用图1所示装置除去Cl2中含有的少量HCl,故A错误;
B.蒸发结晶时应有较多固体是停止加热用余热蒸干,故B错误;
C.氯气与NaOH溶液反应,导致圆底烧瓶内压强减小,可形成喷泉,故C正确;
D.氨气密度比空气小,应用向下排空法收集,故D错误.
故选C.
B.蒸发结晶时应有较多固体是停止加热用余热蒸干,故B错误;
C.氯气与NaOH溶液反应,导致圆底烧瓶内压强减小,可形成喷泉,故C正确;
D.氨气密度比空气小,应用向下排空法收集,故D错误.
故选C.
点评:本题考查实验方案的评价,侧重于物质的分离、制备以及收集,题目难度不大,注意相关物质的性质的把握.

练习册系列答案
相关题目
某温度下,已知反应mX(g)+nY(g)?qZ(g)△H>0,m+n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是( )
A、反应速率v正(X)=
| ||
| B、加入X,反应的△H增大 | ||
| C、增加Y的物质的量,X的转化率增大 | ||
D、降低温度,
|
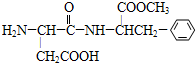 代糖是一种人工合成的甜味剂(sweetener),由于它不会被消化而变为能量共给身体所需,所以适合一些减肥人士食用.目前为止,天冬酰苯丙氨酸甲酯(aspartame)尚未有证据证实它是致癌物质,是糖的最佳代用品,比一般的蔗糖甜160倍.请根据图结构式判断下列关于aspartame的描述正确的是( )
代糖是一种人工合成的甜味剂(sweetener),由于它不会被消化而变为能量共给身体所需,所以适合一些减肥人士食用.目前为止,天冬酰苯丙氨酸甲酯(aspartame)尚未有证据证实它是致癌物质,是糖的最佳代用品,比一般的蔗糖甜160倍.请根据图结构式判断下列关于aspartame的描述正确的是( )| A、是芳香烃 |
| B、分子式是C14H19N2O5 |
| C、具有两性 |
| D、1mol aspartame最多能与3mol NaOH反应 |
化学与生产、生活、社会密切相关.下列有关说法中不正确的是( )
| A、聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 |
| B、使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾 |
| C、植物油和裂化汽油都可以使溴水褪色 |
| D、神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
a、b、c、d四个集气瓶中装有Cl2、H2、HCl、HBr中的一种气体,若a、d两瓶气体混合见光爆炸,a、b两瓶气体混合瓶壁出现暗红色小液滴,则c瓶装的气体是( )
| A、HBr |
| B、HCl |
| C、Cl2 |
| D、H2 |
下列说法正确的是( )
(1)1L0.3mol/LNaHSO4溶液中约含有0.3×6.02×1023个Na+;
(2)9gH2O中约有5×6.02×1023个质子;
(3)11.2LCO2中含有1.5×6.02×1023个原子;
(4)5.6gFe与盐酸完全反应时,失去约0.3×6.02×1023个电子;
(5)500mL0.2mol/LAlCl3溶液中含有0.2×6.02×1023个Cl-.
(1)1L0.3mol/LNaHSO4溶液中约含有0.3×6.02×1023个Na+;
(2)9gH2O中约有5×6.02×1023个质子;
(3)11.2LCO2中含有1.5×6.02×1023个原子;
(4)5.6gFe与盐酸完全反应时,失去约0.3×6.02×1023个电子;
(5)500mL0.2mol/LAlCl3溶液中含有0.2×6.02×1023个Cl-.
| A、(1)(2) |
| B、(1)(2)(3) |
| C、(1)(2)(3)(4) |
| D、(1)(2)(3)(4)(5) |
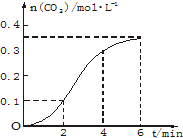 CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图.下列结论正确的是( )
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图.下列结论正确的是( )| A、反应开始4 min内温度对反应速率的影响比浓度小 |
| B、反应4 min后平均反应速率最小 |
| C、反应开始2 min内平均反应速率最大 |
| D、反应在第2 min到第4 min间生成CO2的平均反应速率为 v(CO2)=0.1 mo1?(L?min)-1 |
某单质能和浓硝酸反应,若参加反应的单质与硝酸的物质的量之比为1:4,则组成该单质的元素在产物中的化合价可能是( )
| A、+1 | B、+2 | C、+3 | D、+4 |