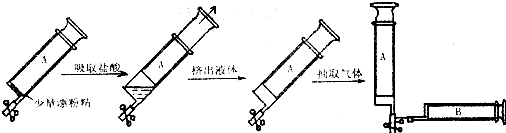
研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且锰化合物的还原产物都是MnCl2.他们将9.48g KMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到标准状况下0.112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,则消耗盐酸的物质的量是( )
| A、0.46mol |
| B、0.4mol |
| C、0.28mol |
| D、无法确定 |
T1℃时,向容积为2L的密闭容器中充入一定量的A气体和B气体,发生如下反应:A(g)+2B (g)?C(g)
反应过程中测定的部分数据见下表:
下列说法正确的是( )
反应过程中测定的部分数据见下表:
| 反应时间/min | n(A)/mol | n(B)/mol |
| 0 | 1.00 | 1.20 |
| 10 | 0.50 | |
| 30 | 0.20 |
| A、前10 min内反应的平均速率为v(C)=0.050 mol?L-1?min-1 |
| B、保持其他条件不变,起始时向容器中充入0.50 mol A气体和0.60 mol B气体,到达平衡时,n(C)<0.25 mol |
| C、温度为T2℃时(T1>T2),上述反应平衡常数为20,则正反应为放热反应 |
| D、其他条件不变,向平衡体系中再充入0.50molA,与原平衡相比,达到新平衡时,B的转化率增大,A的体积分数增大 |
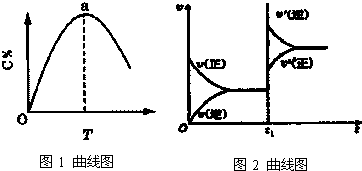
图1表示mA(g)+nB(g)?pC(g)+qD(g)△H=-Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡后t时刻(温度不变)改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是 ( )

| A、m+n>p+q Q>0 |
| B、m+n>p+q Q<0 |
| C、m+n<p+q Q>0 |
| D、m+n<p+q Q<0 |
室温下c(H+)、体积均相同的HCl溶液和CH3COOH溶液分别采取以下措施,有关叙述正确的是
( )
( )
| A、加适量的CH3COONa晶体,两溶液的氢离子浓度都减小 |
| B、使温度升高20℃,两溶液的氢离子浓度都不变 |
| C、与等浓度的NaOH溶液反应,消耗NaOH溶液的体积一样多 |
| D、加足量的Zn充分反应后,两溶液中产生的氢气一样多 |