题目内容
在100mL 36.5%的浓盐酸(密度1.18g/cm3)中加入 mL 2mol/L的稀盐酸(密度1.08g/cm3)才能配成6mol/L的盐酸(密度1.10g/cm3).
考点:物质的量浓度的相关计算
专题:计算题
分析:根据c=
计算浓盐酸物质的量浓度,假设需要2mol/L稀盐酸xmL,根据m=ρV计算混合前各盐酸的质量,进而表示出混合后溶液质量,再根据V=
表示处于混合后溶液的体积,根据HCl的物质的量列方程计算.
| 1000ρw |
| M |
| m |
| ρ |
解答:
解:密度1.18g/cm3、36.5%的浓盐酸物质的量浓度为
mol/L=11.8mol/L,则100mL浓盐酸中HCl为0.1L×11.8mol/L=1.18mol,浓盐酸质量为100mL×1.18g/mL=118g,
假设需要2mol/L稀盐酸xmL,则该盐酸中HCl为0.002x mol,该盐酸质量为xmL×1.08g/mL=1.08x g,
混合后溶液质量为:118g+1.08x g,混合后溶液体积为
,
故1.18mol+0.002x mol=
×6mol/L,
解得x=137.9,
故答案为:137.9.
| 1000×1.18×36.5% |
| 36.5 |
假设需要2mol/L稀盐酸xmL,则该盐酸中HCl为0.002x mol,该盐酸质量为xmL×1.08g/mL=1.08x g,
混合后溶液质量为:118g+1.08x g,混合后溶液体积为
| 118g+1.08xg |
| 1100g/L |
故1.18mol+0.002x mol=
| 118g+1.08xg |
| 1100g/L |
解得x=137.9,
故答案为:137.9.
点评:本题考查物质的量浓度有关计算,注意对公式的理解与灵活应用,题目计算量较大,为易错题目.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
我国歼-10战斗机利用现代科技将
Po涂于飞机表面,可以吸收和屏蔽雷达和红外线辐射,起到一定的隐身作用.该Po(钋)原子核外电子数是( )
209 84 |
| A、209 | B、125 |
| C、84 | D、42 |
下列说法正确的是( )
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 |
| D、天然气、乙醇和水煤气分别属于化石能源、不可再生能源和二次能源 |
图1表示mA(g)+nB(g)?pC(g)+qD(g)△H=-Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡后t时刻(温度不变)改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是 ( )
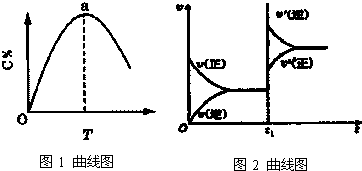

| A、m+n>p+q Q>0 |
| B、m+n>p+q Q<0 |
| C、m+n<p+q Q>0 |
| D、m+n<p+q Q<0 |
向300mL KOH溶液中缓慢通入2.24L(标准状况下)CO2气体,充分反应后,在减压蒸干溶液,得到11.9g白色固体.则下列说法中正确的是( )
| A、此白色固体为KOH和K2CO3的混合物 |
| B、此白色固体中含有K2CO3 6.90g |
| C、原KOH溶液中的物质的量浓度是0.500 mol?L-1 |
| D、此白色固体KHCO3 |
碘可能呈金属性,下列事实能说明这一事实的是( )
| A、已经制得I(NO3)3、I(ClO4)3?2H2O等含I3+的化合物 |
| B、已经制得IBr、ICl 等卤素互化物 |
| C、碘易溶于KI溶液形成I3- |
| D、I4O9可以看成是碘酸盐 |
 .请写出A与稀、冷的KMnO4溶液在碱性
.请写出A与稀、冷的KMnO4溶液在碱性