50g镁、锌、铁的混合物与足量的稀硫酸反应得到混合溶液,蒸发得到218g固体(换算为无水硫酸盐).则反应产生氢气的质量是( )
| A、3.5g | B、3g |
| C、2g | D、4.5g |
下列各组物质仅用蒸馏水不能鉴别出的是( )
| A、苯、酒精、硝基苯 |
| B、氧化铜、二氧化锰、活性碳 |
| C、食盐、烧碱、硝酸铵 |
| D、蔗糖、硫酸铜粉末、碳酸钙粉末 |
由CO、CH4和C2H2组成的混合气体4.48L(标况),在足量氧气中充分燃烧后,生成的气体先通过足量的浓H2SO4再通过足量的NaOH溶液,NaOH溶液增重13.2g,则混合气体中含C2H2的物质的量n为( )
| A、n<0.1mol |
| B、n=0.1mol |
| C、0.1mol<n<0.15mol |
| D、无法确定 |
一定体积0.01mol/L的稀硝酸溶液恰好能氧化一定质量的铁、铝混合物,已知两种金属均被氧化为最高价态,还原产物只有NO.若用0.01mol/L NaOH溶液溶解相同质量的该混合物,当反应完全时所需氢氧化钠溶液的体积是稀硝酸溶液的1/5,则样品中铁、铝的物质的量之比为( )
| A、1:4 | B、1:3 |
| C、2:3 | D、5:3 |
两种气态烃的混合气共1mol,在空气中燃烧得到1.5molCO2和2molH2O.关于该混合气的说法合理的是( )
| A、一定含甲烷,不含乙烷 |
| B、一定含乙烷,不含甲烷 |
| C、可能是甲烷和乙烯的混合物 |
| D、一定含甲烷,但不含乙烯 |
今有H2和CO(体积比为1:2)的混合气体V L,完全燃烧时,所需要同条件O2的体积为( )
| A、3V L |
| B、2V L |
| C、V L |
| D、0.5V L |
1L0.1mol?L-1 AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极增重2.16g时,下列判断正确的是(设电解按理论进行,溶液不蒸发)( )
| A、转移的电子数是1.204×1022 |
| B、阳极上产生112mLO2(标准状况) |
| C、溶液的浓度变化为0.08mol?L-1 |
| D、反应中有0.01molAg被氧化 |
将2.24L甲烷(标况)和一定量氧气混合燃烧,得产物CO、CO2和水蒸气共7.2g,当其缓慢经过无水CaCl2时,CaCl2增重3.6g,原混合气体中CO2的质量为( )
| A、2.31g | B、4.4g |
| C、3.3g | D、2.2g |
 常温下用惰性电极电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(以下气体体积已换算成标准状况下的体积).根据图中信息回答下列问题.
常温下用惰性电极电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(以下气体体积已换算成标准状况下的体积).根据图中信息回答下列问题.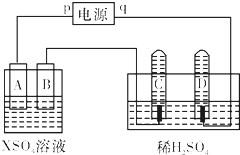 如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡.试回答:
如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡.试回答: