题目内容
今有H2和CO(体积比为1:2)的混合气体V L,完全燃烧时,所需要同条件O2的体积为( )
| A、3V L |
| B、2V L |
| C、V L |
| D、0.5V L |
考点:有关混合物反应的计算
专题:计算题
分析:发生反应:2H2+O2
2H2O、2CO+O2
2CO2,2体积H2、2体积CO燃烧都消耗1体积氧气,据此计算.
| ||
| ||
解答:
解:发生反应:2H2+O2
2H2O、2CO+O2
2CO2,2体积H2、2体积CO燃烧都消耗1体积氧气,故H2和CO(体积比为1:2)的混合气体V L,完全燃烧时,所需要同条件O2的体积为VL×
=0.5V L,故选D.
| ||
| ||
| 1 |
| 2 |
点评:本题考查混合物计算,比较基础,注意利用方程式进行解答.

练习册系列答案
相关题目
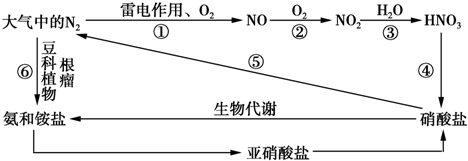
在反应5NH4NO3
2HNO3+4N2↑+9H2O中,发生氧化的氮原子与发生还原的氮原子的物质的量之比为( )
| ||
| A、3:5 | B、5:3 |
| C、5:8 | D、5:4 |
下列反应的离子方程式正确的是( )
A、乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+OH-
| ||
B、向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-
| ||
| C、苯酚钠溶液中通入少量二氧化碳:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | ||
D、乙醛溶液与新制氢氧化铜碱性悬浊液共热CH3CHO+2Cu(OH)2+OH-
|
下列家庭化学小实验不能达到预期目的是( )
| A、用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物 |
| B、用食醋、石灰水验证蛋壳中含有碳酸盐 |
| C、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| D、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
下列各组物质仅用蒸馏水不能鉴别出的是( )
| A、苯、酒精、硝基苯 |
| B、氧化铜、二氧化锰、活性碳 |
| C、食盐、烧碱、硝酸铵 |
| D、蔗糖、硫酸铜粉末、碳酸钙粉末 |
将一定质量的铁、铜组成的混合物9.90g加入到稀硝酸中,金属完全溶解(假设反应中还原产物全部是NO).向反应后的溶液中加入6mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加到17.55g,则下列叙述中正确的是( )
| A、当金属全部溶解时收集到NO气体的体积为3.36L |
| B、当金属全部溶解时,无法计算参加反应的硝酸的物质的量 |
| C、将生成的沉淀加热灼烧,可能得到FeO、Fe2O3和CuO的混合物 |
| D、当生成沉淀达到最大量时,消耗NaOH溶液的体积为V≥75ml |
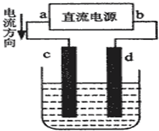 如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )
如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )| A、a为负极、b为正极 |
| B、电解过程中,c电极发生还原反应 |
| C、电解过程中,d电极质量增加 |
| D、电解过程中,氯离子浓度不变 |