某学生配制一定物质的量浓度的氢氧化钠溶液后,经测定发现溶液浓度偏低.该学生找出以下原因,其中不会使溶液浓度偏低的是( )
| A、容量瓶刚用蒸馏水洗净,没有烘干 |
| B、没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中 |
| C、定容时滴加蒸馏水先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 |
| D、定容时仰视刻度线 |
下列关于实验原理或操作的叙述中,正确的是( )
| A、NaCl溶液蒸发结晶时,蒸发皿中有大量晶体析出即停止加热 |
| B、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C、在50mL量筒中配制0.10mol/L的碳酸钠溶液 |
| D、将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
下列行为中符合安全要求的是( )
| A、节日期间,在开阔的广场燃放烟花爆竹 |
| B、进入煤矿井时,用火把照明 |
| C、用点燃的火柴在液化气钢瓶口检验是否漏气 |
| D、稀释浓硫酸时,将水倒入装浓硫酸的烧杯中 |
amolNa2O2和b mol NaHCO3固体混合后,在密闭容器中加热到2500C,使其充分反应,当排出O2和H2O的物质的量为1:1时,a:b为( )
| A、1:1 | B、1:2 |
| C、2:3 | D、2:1 |
为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入( )
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸.
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸.
| A、①② | B、③④ | C、①③ | D、②④ |

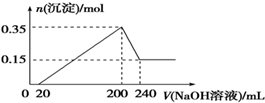 通过计算得到:
通过计算得到: