题目内容
为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入( )
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸.
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸.
| A、①② | B、③④ | C、①③ | D、②④ |
考点:物质分离、提纯的实验方案设计
专题:实验设计题
分析:CO2混有HCl和水,应先除去HCl,可用饱和NaHCO3溶液,二氧化碳为酸性气体,可用酸性或中性干燥剂干燥.
解答:
解:①CO2不溶于饱和NaHCO3溶液,HCl与饱和NaHCO3溶液反应生成CO2而除去,可用无水CaCl2干燥,故正确;
②CO2不溶于饱和NaHCO3溶液,HCl与饱和NaHCO3溶液反应生成CO2而除去,可用浓硫酸干燥,故正确;
③后通入饱和NaHCO3溶液,不能除去水蒸气,错误;
④稀硫酸不具有干燥的作用,故错误.
故选A.
②CO2不溶于饱和NaHCO3溶液,HCl与饱和NaHCO3溶液反应生成CO2而除去,可用浓硫酸干燥,故正确;
③后通入饱和NaHCO3溶液,不能除去水蒸气,错误;
④稀硫酸不具有干燥的作用,故错误.
故选A.
点评:本题考查气体的净化和干燥,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握物质的性质,除杂时不能影响被提纯的物质.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
用过量的H2SO4、NaOH、NH3?H2O、NaCl等溶液,按如图步骤分开五种离子,则溶液①、②、③、④是( )


| A、①NaCl ②NaOH ③NH3?H2O ④H2SO4 |
| B、①NaCl ②NH3?H2O ③NaOH ④H2SO4 |
| C、①H2SO4 ②NH3?H2O ③NaOH ④NaCl |
| D、①H2SO4 ②NaOH ③NH3?H2O ④NaCl |
在容积相同的甲、乙两个密闭容器中,均分别充入2mol SO2和1mol O2,发生反应:2SO2+O2?2SO3,在相同温度下,若甲容器始终保持体积不变,乙容器始终保持压强不变,达平衡时测得甲容器中SO2的转化率为25%,则乙容器中SO2的转化率( )
| A、25% | B、小于25% |
| C、大于25% | D、无法确定 |
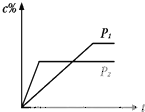 在温度相同,压强分别为P1和P2的条件下,2A(g)+B(s)?nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是( )
在温度相同,压强分别为P1和P2的条件下,2A(g)+B(s)?nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是( )| A、P1>P2,n<3 |
| B、P1<P2,n>2 |
| C、P1>P2,n>3 |
| D、P1<P2,n<2 |
下列有关实验的叙述中,正确的是( )
| A、容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液 |
| B、用分液的方法分离水和酒精的混合物 |
| C、配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体 |
| D、用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁 |
如图所示的操作,其中正确的是( )
A、 收集干燥二氧化碳 |
B、 检查装置的气密性 |
C、 加入药品 |
D、 除去CO中CO2 |
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
| A、生成42.0LN2(标准状况) |
| B、转移电子的物质的量为1.25mol |
| C、有0.250molKNO3被氧化 |
| D、被氧化的N原子的物质的量为1.875mol |
某实验室的尾气中含有较多的氯气,有毒,要吸收这些尾气,下列试剂最适合的是( )
| A、自来水 | B、饱和食盐水 |
| C、饱和石灰水 | D、烧碱溶液 |
