题目内容
下列关于实验原理或操作的叙述中,正确的是( )
| A、NaCl溶液蒸发结晶时,蒸发皿中有大量晶体析出即停止加热 |
| B、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C、在50mL量筒中配制0.10mol/L的碳酸钠溶液 |
| D、将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
考点:分液和萃取,过滤,蒸发和结晶、重结晶
专题:化学实验基本操作
分析:A.蒸发时,利用余热蒸干溶液;
B.根据萃取剂的密度判断有机层的位置,从而判断出口方向;
C.量筒不能用来配制溶液;
D.过滤时应该用玻璃棒引流.
B.根据萃取剂的密度判断有机层的位置,从而判断出口方向;
C.量筒不能用来配制溶液;
D.过滤时应该用玻璃棒引流.
解答:
解:A.蒸发时,当蒸发皿中有大量晶体析出时就停止加热,利用余热蒸干,故A正确;
B.苯的密度比水小,故溴的苯溶液在上层,应从上口倒出,故B错误;
C.量筒不能用来配制溶液,应用容量瓶,故C错误;
D.过滤时应该用玻璃棒引流,否则易溅出液体或弄坏滤纸,故D错误.
故选A.
B.苯的密度比水小,故溴的苯溶液在上层,应从上口倒出,故B错误;
C.量筒不能用来配制溶液,应用容量瓶,故C错误;
D.过滤时应该用玻璃棒引流,否则易溅出液体或弄坏滤纸,故D错误.
故选A.
点评:本题考查基本实验操作,难度不大,易错选项是D,明确过滤中玻璃棒的作用,为易错点.

练习册系列答案
相关题目
某有机物完全燃烧,生成的产物只有CO2和H2O.将6g该有机物完全燃烧的产物通过浓硫酸,浓硫酸增重7.2g,再通过氢氧化钠溶液,又增重13.2g.该有机物的分子式为( )
| A、C4H10 |
| B、C3H8 |
| C、C3H8O |
| D、C2H4O2 |
据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应的化学方程式为:2CO2(g)+6H2(g)═CH3CH2OH(g)+3H2O(g).下列叙述正确的是( )
| A、当v(CO2)=2v(CH3CH2OH)时,反应一定达到平衡状态 |
| B、增大压强,可提高CO2和H2的转化率 |
| C、当平衡向正反应方向移动时,平衡常数一定增大 |
| D、移去生成的乙醇和水,可以加快反应速率 |
完成下列实验,所选装置正确的是( )
| A | B | C | D | |
| 实验 目的 | 实验室 制备乙烯 | 分离苯和溴苯的混合物(沸点:苯为80.1℃,溴苯为156.2℃) | 分离KCl和NH4Cl固体混合物 | 实验室用纯碱和稀硫酸制备二氧化碳 |
| 实验装置 |  |  | 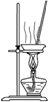 | 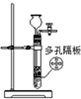 |
| A、A | B、B | C、C | D、D |
将自来水加工成蒸馏水过程中,没有涉及到的过程或变化是( )
| A、化学变化 | B、冷凝 |
| C、蒸发 | D、物理变化 |
现有三组溶液,①汽油和氯化钠溶液,②乙醇和CCl4的混合物,③氯化钠和单质碘的水溶液.分离以上各混合物的正确方法依次是( )
| A、分液、萃取、蒸馏 |
| B、萃取、蒸馏、分液 |
| C、分液、蒸馏、萃取 |
| D、蒸馏、萃取、分液 |
在元素周期表中,对于相同主族相邻周期的两种元素原子序数之差的叙述正确的是( )
| A、第2、3周期两元素相差均为8 |
| B、第3、4周期两元素相差均为18 |
| C、第5、6周期两元素相差均为32 |
| D、以上叙述均正确 |