题目内容
amolNa2O2和b mol NaHCO3固体混合后,在密闭容器中加热到2500C,使其充分反应,当排出O2和H2O的物质的量为1:1时,a:b为( )
| A、1:1 | B、1:2 |
| C、2:3 | D、2:1 |
考点:化学方程式的有关计算
专题:计算题
分析:混合物在密闭容器中加热到250℃时,可能发生如下反应:
①2NaHCO3
Na2CO3+CO2↑+H2O↑
②2Na2O2+2CO2=2Na2CO3+O2
③2Na2O2+2H2O=4NaOH+O2
④2NaOH+CO2=Na2CO3+H2O?
由上述反应,可得总的反应方程式为:
Ⅰ、Na2O2+2NaHCO3
2Na2CO3+
O2↑+H2O↑
Ⅱ、2Na2O2+2NaHCO3
2Na2CO3+O2↑+2NaOH
当排出O2和H2O的物质的量为1:1时,只能发生反应Ⅰ、Ⅱ,根据方程式计算解答.
①2NaHCO3
| ||
②2Na2O2+2CO2=2Na2CO3+O2
③2Na2O2+2H2O=4NaOH+O2
④2NaOH+CO2=Na2CO3+H2O?
由上述反应,可得总的反应方程式为:
Ⅰ、Na2O2+2NaHCO3
| ||
| 1 |
| 2 |
Ⅱ、2Na2O2+2NaHCO3
| ||
当排出O2和H2O的物质的量为1:1时,只能发生反应Ⅰ、Ⅱ,根据方程式计算解答.
解答:
解:混合物在密闭容器中加热到250℃时,可能发生如下反应:
①2NaHCO3
Na2CO3+CO2↑+H2O↑
②2Na2O2+2CO2=2Na2CO3+O2
③2Na2O2+2H2O=4NaOH+O2
④2NaOH+CO2=Na2CO3+H2O?
由上述反应,可得总的反应方程式为:
Ⅰ、Na2O2+2NaHCO3
2Na2CO3+
O2↑+H2O↑
Ⅱ、2Na2O2+2NaHCO3
2Na2CO3+O2↑+2NaOH
当排出O2和H2O的物质的量为1:1时,只能发生反应Ⅰ、Ⅱ,
Ⅰ×2+Ⅱ可得:4Na2O2+6NaHCO3
6Na2CO3+2O2↑+2NaOH+2H2O↑
故n(Na2O2):n(NaHCO3)=4:6=2:3,
故选C.
①2NaHCO3
| ||
②2Na2O2+2CO2=2Na2CO3+O2
③2Na2O2+2H2O=4NaOH+O2
④2NaOH+CO2=Na2CO3+H2O?
由上述反应,可得总的反应方程式为:
Ⅰ、Na2O2+2NaHCO3
| ||
| 1 |
| 2 |
Ⅱ、2Na2O2+2NaHCO3
| ||
当排出O2和H2O的物质的量为1:1时,只能发生反应Ⅰ、Ⅱ,
Ⅰ×2+Ⅱ可得:4Na2O2+6NaHCO3
| ||
故n(Na2O2):n(NaHCO3)=4:6=2:3,
故选C.
点评:本题考查混合物的有关计算、钠的化合物的性质等,难度较大,注意利用方程式叠加讨论剩余固体、排出的气体发生的反应情况.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
一定条件下,在2L的密闭容器中发生可逆反应:Fe(s)+CO(g)?Fe(s)+CO2(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲,图乙是T1温度下该反应的c-t关系图象.则下列说法正确的是( )


| A、保持恒容恒温条件,向密闭容器中充入氦气,化学反应速率将变快 |
| B、若容器的容积不变,降低温度,c(CO2)/c(CO)减小 |
| C、保持恒容恒温(T1)条件,8min达化学平衡状态时,v(CO)=0.0625mol/(L?s) |
| D、保持恒容恒温(T1)条件,8min后再加入足量FeO粉末并充入1.5mol的CO气体,重新达到平衡时,CO的转化率为33.3% |
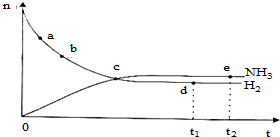 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)═2NH3(g)△H<0,673K,30M Pa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)═2NH3(g)△H<0,673K,30M Pa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )| A、点a的正反应速率比点b的大 |
| B、点c处反应达到平衡 |
| C、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D、点c处用氨气的浓度表示的速率等于用氢气的浓度表示的速率 |
某学生配制一定物质的量浓度的氢氧化钠溶液后,经测定发现溶液浓度偏低.该学生找出以下原因,其中不会使溶液浓度偏低的是( )
| A、容量瓶刚用蒸馏水洗净,没有烘干 |
| B、没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中 |
| C、定容时滴加蒸馏水先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 |
| D、定容时仰视刻度线 |
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一.对下列实验事实的解释不正确的是( )
| A、某溶液中加入稀硫酸再加入铜粉,共热,铜粉溶解且有红棕色气体产生,说明原溶液中含有NO3- |
| B、浓硝酸在光照条件下变黄,说明浓硝酸不稳定,有有色产物生成且能溶于浓硝酸 |
| C、某溶液中加入NaOH溶液,加热能产生使湿润的红色石蕊试纸变蓝的气体,说明原溶液中含有NH4+ |
| D、在KI淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应 |