如图为反应N2+3H2?2NH3的速率V(N2)变化的图象,则横坐标不可能是( )


| A、反应时间 |
| B、温度 |
| C、压强 |
| D、N2的浓度 |
下列叙述中,正确的是( )
| A、如果加四氯化碳呈现紫色,证明原溶液中存在I- |
| B、加入盐酸产生白色沉淀的溶液一定是硝酸银溶液 |
| C、二氧化硅是酸性氧化物,能够与水反应生成酸 |
| D、氢氟酸是弱酸,但会腐蚀玻璃 |
实验要快速制取H2,最好的方法是( )
| A、纯锌和稀H2SO4反应 |
| B、纯锌和浓硫酸反应 |
| C、粗锌和浓H2SO4反应 |
| D、粗锌和稀硫酸反应 |
下列4支试管中,等质量的铁与足量等体积的盐酸反应生成H2的反应速率最大的是( )
| 试管 | 盐酸浓度(mol?L-1) | 温度(℃) | 铁的状态 |
| A | 1.0 | 20 | 块状 |
| B | 1.0 | 20 | 粉末状 |
| C | 3.0 | 30 | 块状 |
| D | 3.0 | 30 | 粉末状 |
| A、A | B、B | C、C | D、D |
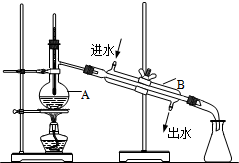 如图为实验室制取自来水的装置示意图,根据图示回答下列问题.
如图为实验室制取自来水的装置示意图,根据图示回答下列问题.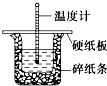 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中的热量可计算中和热.回答下列问题:
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中的热量可计算中和热.回答下列问题: 汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究小组在实验室以Ag-ZSM-5 为催化剂,测得NO转化为N2的转化率随温度变化情况如图.
汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究小组在实验室以Ag-ZSM-5 为催化剂,测得NO转化为N2的转化率随温度变化情况如图. 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.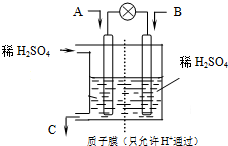 所以“低碳经济”正成为科学家研究的主要课题.
所以“低碳经济”正成为科学家研究的主要课题.