题目内容
 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.Ⅰ.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体
(2)配制过程中需要用到的玻璃仪器除烧杯、玻璃棒外还需要有
Ⅱ.测定中和热的实验装置如图所示.
(3)大小烧杯之间填满碎泡沫塑料的作用是
(4)使用补全仪器后的装置进行实验,取50mL 0.25mol/L H2SO4溶液与50mL0.55mol/L NaOH溶液在小烧杯中进行中和反应,实验数据如表.
| 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②通过计算可得中和热△H=
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(5)实验中若用60mL0.25mol?L-1H2SO4溶液跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
考点:中和热的测定
专题:化学反应中的能量变化
分析:Ⅰ.(1)根据公式m=nM=cVM来计算氢氧化钠的质量,但是没有245mL的容量瓶;
(2)需要用到的玻璃仪器有烧杯、容量瓶、胶头滴管和玻璃棒;
Ⅱ.(3)中和热测定实验成败的关键是保温工作;根据量热计的构造来判断该装置的缺少仪器;(4)①先判断温度差的有效性,然后求出温度差平均值;
②根据公式Q=△H=△Tcm来计算反应的焓变;
③a.装置保温、隔热效果差,测得的热量偏小;
b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,放出的热量偏高;
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中,热量散失较多;
d.温度计测定NaOH溶液起始温度后直接插入稀H2SO4测温度,硫酸的起始温度偏高;
(5)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答.
(2)需要用到的玻璃仪器有烧杯、容量瓶、胶头滴管和玻璃棒;
Ⅱ.(3)中和热测定实验成败的关键是保温工作;根据量热计的构造来判断该装置的缺少仪器;(4)①先判断温度差的有效性,然后求出温度差平均值;
②根据公式Q=△H=△Tcm来计算反应的焓变;
③a.装置保温、隔热效果差,测得的热量偏小;
b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,放出的热量偏高;
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中,热量散失较多;
d.温度计测定NaOH溶液起始温度后直接插入稀H2SO4测温度,硫酸的起始温度偏高;
(5)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答.
解答:
解:Ⅰ.(1)容量瓶没有245mL规格的,只能用250mL规格的,需要称量NaOH固体m=nM=cVM=0.5mol/L×0.25L×40g/mol=5.0g,故答案为:5.0;
(2)配制0.50mol/L NaOH溶液需要用到的玻璃仪器有烧杯、250mL容量瓶、胶头滴管和玻璃棒,故答案为:250mL容量瓶;胶头滴管;
Ⅱ.(3)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失;由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;
故答案为:减少实验过程中的热量损失;环形玻璃搅拌棒;
(4)①4次温度差分别为:3.4℃,6.1℃,3.3℃,3.5℃,第二组数据舍去,三次温度差平均值=
=3.4℃,故答案为:3.4;
②Q=△H=-△Tcm=-3.4°C×4.18J/(g?℃)×100g═1421.2J=1.42KJ/mol,△H=-
(H2O)=-56.8KJ/mol,故答案为:-56.8kJ?mol-1;
③a.装置保温、隔热效果差,测得的热量偏小,中和热的数值偏小,故a正确;
b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,放出的热量偏高,中和热的数值偏大,故b错误;
b.分多次把NaOH 溶液倒人盛有硫酸的小烧杯中,热量散失较多,测得温度偏低,中和热的数值偏小,故c正确;
b.温度计测定NaOH溶液起始温度后直接插入稀H2SO4测温度,硫酸的起始温度偏高,测得的热量偏小,中和热的数值偏小,故d正确,
故答案为:acd;
(5)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25mol?L-1H2SO4溶液跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,中和热相等;又醋酸是弱酸,电离过程吸热,所以用50mL0.50mol?L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会减小,
故答案为:不相等;相等;偏小.
(2)配制0.50mol/L NaOH溶液需要用到的玻璃仪器有烧杯、250mL容量瓶、胶头滴管和玻璃棒,故答案为:250mL容量瓶;胶头滴管;
Ⅱ.(3)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失;由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;
故答案为:减少实验过程中的热量损失;环形玻璃搅拌棒;
(4)①4次温度差分别为:3.4℃,6.1℃,3.3℃,3.5℃,第二组数据舍去,三次温度差平均值=
| 3.4℃+3.3℃+3.5℃ |
| 3 |
②Q=△H=-△Tcm=-3.4°C×4.18J/(g?℃)×100g═1421.2J=1.42KJ/mol,△H=-
| Q |
| N |
③a.装置保温、隔热效果差,测得的热量偏小,中和热的数值偏小,故a正确;
b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,放出的热量偏高,中和热的数值偏大,故b错误;
b.分多次把NaOH 溶液倒人盛有硫酸的小烧杯中,热量散失较多,测得温度偏低,中和热的数值偏小,故c正确;
b.温度计测定NaOH溶液起始温度后直接插入稀H2SO4测温度,硫酸的起始温度偏高,测得的热量偏小,中和热的数值偏小,故d正确,
故答案为:acd;
(5)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25mol?L-1H2SO4溶液跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,中和热相等;又醋酸是弱酸,电离过程吸热,所以用50mL0.50mol?L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会减小,
故答案为:不相等;相等;偏小.
点评:本题考查热中和热概念、测定原理及反应热的计算,题目难度大,注意理解中和热的概念以及测定反应热的误差等问题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如表:下列说法错误的是( )
| 物质 | X | T | Z |
| 初始浓度/mol?L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、反应达到平衡时,X的转化率为50% |
| B、反应可表示为X+3Y?2Z,其平衡常数为1600(mol/L)-2 |
| C、改变温度可以改变此反应的平衡常数 |
| D、增大压强使平衡向生成Z的方向移动,平衡常数增大 |
下列4支试管中,等质量的铁与足量等体积的盐酸反应生成H2的反应速率最大的是( )
| 试管 | 盐酸浓度(mol?L-1) | 温度(℃) | 铁的状态 |
| A | 1.0 | 20 | 块状 |
| B | 1.0 | 20 | 粉末状 |
| C | 3.0 | 30 | 块状 |
| D | 3.0 | 30 | 粉末状 |
| A、A | B、B | C、C | D、D |
下列确定某溶液中一定有SO
的方法中,正确的是( )
2- 4 |
| A、先加BaCl2溶液有白色沉淀,再加稀盐酸沉淀不消失 |
| B、先加BaCl2溶液有白色沉淀,再加稀硝酸沉淀不消失 |
| C、先加Ba(NO3)2溶液有白色沉淀,再加稀盐酸沉淀不消失 |
| D、先加稀盐酸无明显现象,再加BaCl2溶液有白色沉淀 |
向10mL 0.1mol/L Na2CO3溶液中逐滴滴加V mL 0.1mol/L HCl溶液,下列有关滴定过程中粒子浓度关系正确的是( )
| A、当V=0时,[OH-]=[H+]+[HCO3-]+2[H2CO3] |
| B、当V=5时,[Na+]+[H+]=2[CO32-]+[HCO3-]+[OH-] |
| C、当V=10时,[Cl-]=[CO32-]+[HCO3-]+[H2CO3] |
| D、当V=15时,[Na+]=[Cl-]>[HCO3-]>[OH-]>[H+] |
 实验室里需用480mL 0.1mol?L-1的硫酸铜溶液.试回答该溶液配制过程中的下列问题:
实验室里需用480mL 0.1mol?L-1的硫酸铜溶液.试回答该溶液配制过程中的下列问题: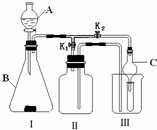 某研究性学习小组设计的实验装置(如图),既可用于制取气体,又可用于验证物质性质.
某研究性学习小组设计的实验装置(如图),既可用于制取气体,又可用于验证物质性质.