在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型为( )
| A、正十二面体 | B、正八面体 |
| C、正六面体 | D、正四面体 |
NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A、O2和O3共32 g混合物中氧原子的个数为2NA |
| B、78 g苯含有C═C 键的数目为3NA |
| C、1 mol Na2O2固体中含离子总数为4NA |
| D、足量Fe与1 mol 氯气反应时转移的电子数为3NA |
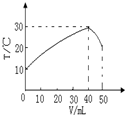 向盛有50mL1.00mol?L-1HCl溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列不正确的是( )
向盛有50mL1.00mol?L-1HCl溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列不正确的是( )| A、该实验表明化学能可以转化为热能 |
| B、NaOH溶液的浓度大于1.00mol?L-1 |
| C、V=50mL时,混合液的pH>7 |
| D、该实验表明有水生成的反应都是放热反应 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温常压下,14 g CO中含有的原子数目为NA |
| B、标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2 NA |
| C、25℃时,pH=13的1.0 L的Ba(OH)2溶液中含有的OH-数目为0.2 NA |
| D、1L1mol?L-1的NaClO 溶液中含有ClO-的数目为NA |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、23 g钠在氧气中完全燃烧失电子数为0.5NA |
| B、46gNO2和N2O4混合气体中含有氮原子数为1NA~2NA |
| C、标准状况下,11.2L的SO3所含分子数为0.5 NA |
| D、室温下,16g甲烷含有共价键数为4 NA |
根据下列反应的化学方程式:①Zn+CuSO4=ZnSO4+Cu、②Cu+2AgNO3=Cu(NO3)2+2Ag,判断三种金属的氧化性强弱顺序是( )
| A、Zn2+>Cu2+>Ag+ |
| B、Zn2+>Ag+>Cu2+ |
| C、Cu2+>Ag+>Zn2+ |
| D、Ag+>Cu2+>Zn2+ |
下列说法错误的是( )
| A、化学反应中的能量变化都表现为热量变化 |
| B、需要加热才能发生的反应不一定是吸热反应 |
| C、向醋酸钠溶液中滴入酚酞试液,加热后若溶液红色加深,则说明盐类水解是吸热的 |
| D、反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
下列说法不正确的是( )
| A、需要加热方能发生的反应不一定是吸热反应 |
| B、反应是吸热还是放热取决于反应物和生成物所具有的总能量的相对大小 |
| C、测定中和反应的反应热时,酸碱中和之后应读取体系达到的最高温度 |
| D、硫在氧气中燃烧,该反应反应产物的总焓大于反应物的总焓 |
下列物质的分类中,前者是电解质,后者是非电解质的组合是( )
| A、AgCl、Cl2 |
| B、NaHCO3、NH3 |
| C、Ba(OH)2、HCl |
| D、H2SO4、盐酸 |