题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、23 g钠在氧气中完全燃烧失电子数为0.5NA |
| B、46gNO2和N2O4混合气体中含有氮原子数为1NA~2NA |
| C、标准状况下,11.2L的SO3所含分子数为0.5 NA |
| D、室温下,16g甲烷含有共价键数为4 NA |
考点:阿伏加德罗常数
专题:
分析:A.钠为1价金属,1mol钠完全反应失去1mol电子;
B.NO2和N2O4的最简式为NO2,根据最简式计算出混合物中含有的氮原子数;
C.标准状况下,三氧化硫不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
D.甲烷分子中含有4个碳氢键,1mol甲烷分子中含有4mol碳氢键共价键.
B.NO2和N2O4的最简式为NO2,根据最简式计算出混合物中含有的氮原子数;
C.标准状况下,三氧化硫不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
D.甲烷分子中含有4个碳氢键,1mol甲烷分子中含有4mol碳氢键共价键.
解答:
解:A.23g钠的物质的量为1mol,1mol钠完全反应失去1mol电子,失电子数为NA,故A错误;
B.46gNO2和N2O4的混合物中含有1mol最简式NO2,含有1mol氮原子,含有氮原子数为1NA,故B错误;
C.标况下三氧化硫不是气体,不能使用标况下的气体摩尔体积计算11.2L三氧化硫的物质的量,故C错误;
D.16g甲烷的物质的量为1mol,1mol甲烷分子中含有4mol碳氢键共价键,含有共价键数为4 NA,故D正确;
故选D.
B.46gNO2和N2O4的混合物中含有1mol最简式NO2,含有1mol氮原子,含有氮原子数为1NA,故B错误;
C.标况下三氧化硫不是气体,不能使用标况下的气体摩尔体积计算11.2L三氧化硫的物质的量,故C错误;
D.16g甲烷的物质的量为1mol,1mol甲烷分子中含有4mol碳氢键共价键,含有共价键数为4 NA,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型为( )
| A、正十二面体 | B、正八面体 |
| C、正六面体 | D、正四面体 |
胶体区别于其它分散系的本质特征是( )
| A、胶体有丁达尔效应 |
| B、胶体粒子带电荷 |
| C、胶体粒子不能穿过半透膜 |
| D、胶体粒子直径在1-100nm之间 |
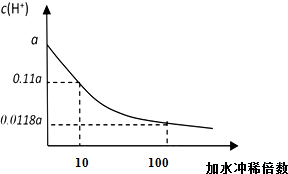 某HA的稀溶液,其浓度为b mol/L,在稀释过程中的c(H+)变化如图所示.
某HA的稀溶液,其浓度为b mol/L,在稀释过程中的c(H+)变化如图所示.