某小组为研究原电池原理,设计如图Ⅰ、Ⅱ装置,下列叙述正确的是( )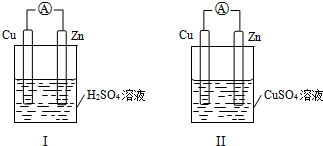

| A、装置Ⅰ,铜片上有O2逸出 |
| B、装置Ⅰ,锌片溶解,发生还原反应 |
| C、装置Ⅱ,电池反应为:Zn+Cu2+=Zn2++Cu |
| D、装置Ⅱ,外电路中,电子从铜电极流向锌电极 |
一定条件下,容积为2L的恒容密闭容器中,通入2mol N2、3mol H2进行反应催化剂高温高压N2(g)+3H2(g)?2NH3(g),20min后,N2的物质的量为1.9mol,1h后测得容器内气体的压强不再改变,且为反应开始时压强的0.8倍,则下列叙述正确的是( )
| A、1 h后反应进行完全,容器中的N2浓度为0.55 mol?L-1 |
| B、前20 min用NH3表示的反应速率为0.01 mol?L-1?min-1 |
| C、增加H2的浓度或降低温度,平衡将向正反应方向移动,且反应速率均加快 |
| D、当容器内压强不改变时,说明反应已达到平衡状态 |
在密闭容器中发生下列反应aA(g)?cC(g)+dD(g),反应达平衡后,将容器体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
| A、A的转化率变小 |
| B、平衡向正反应方向移动 |
| C、D的物质的量变大 |
| D、a>c+d |
 室温下,用0.100mol/L 盐酸溶液滴定20.00mL 0.100mol/L的某氨水溶液,滴定曲线如图所示,下列有关说法不正确的是( )
室温下,用0.100mol/L 盐酸溶液滴定20.00mL 0.100mol/L的某氨水溶液,滴定曲线如图所示,下列有关说法不正确的是( )| A、曲线上除d点外任意一点所示溶液中:c(NH4+)+c(H+)=c(Cl- )+c(OH - ) |
| B、a点所示溶液中,c(Cl-)>c(NH4+ )>c(NH3?H2O)>c(OH- )>c(H+ ) |
| C、b点所示溶液中,c(NH4+)=c(Cl-) |
| D、c点所示溶液中,c(Cl- )>c(NH4+)>c(H+)>c(NH3?H2O) |
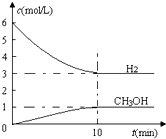 T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得H2和CH3OH(g)的浓度随时间变化如下图所示.下列说法不正确的是( )
T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得H2和CH3OH(g)的浓度随时间变化如下图所示.下列说法不正确的是( )| A、0~10 min 内υ(H2)=0.3 mol/(L?min) | ||
B、T℃时,平衡常数K=
| ||
| C、T℃时,若上述反应中有64 g CH3OH生成,则同时放出98.0 kJ的热量 | ||
| D、达到平衡后,升高温度或再充入CO2气体,都可以提高H2的转化率 |
在一定温度下,反应3A2(g)+B2(g)?4C(g)达到平衡的标志是( )
| A、单位时间生成3nmolA2的同时生成nmolB2 |
| B、c(A2):c(B2):c(C)=3:1:4 |
| C、单位时间生成4nmolC的同时生成nmolB2 |
| D、混合气体的压强不变 |
已建立平衡的某可逆反应,当改变条件,平衡向正反应方向移动时,下列叙述正确的是( )
①生成物的百分含量一定增加
②反应物的转化率一定增加
③反应物的浓度一定降低
④正反应速率一定大于逆反应速率
⑤使用了催化剂.
①生成物的百分含量一定增加
②反应物的转化率一定增加
③反应物的浓度一定降低
④正反应速率一定大于逆反应速率
⑤使用了催化剂.
| A、①② | B、②⑤ | C、⑤ | D、④ |