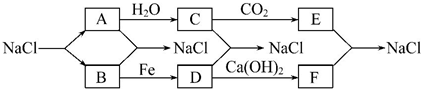
题目内容
某小组为研究原电池原理,设计如图Ⅰ、Ⅱ装置,下列叙述正确的是( )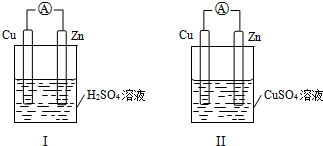

| A、装置Ⅰ,铜片上有O2逸出 |
| B、装置Ⅰ,锌片溶解,发生还原反应 |
| C、装置Ⅱ,电池反应为:Zn+Cu2+=Zn2++Cu |
| D、装置Ⅱ,外电路中,电子从铜电极流向锌电极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:锌比铜活泼,形成原电池时,锌为负极,铜为正极,负极发生氧化反应,电极反应为Zn-2e-=Zn2+,正极发生还原反应,如电解质溶液为硫酸铜,则发生Cu2++2e-=Cu,电解质溶液为硫酸,则发生2H++2e-=H2↑,以此解答该题.
解答:
解:A.装置I,铜片上发生2H++2e-=H2↑,有H2逸出,故A错误;
B.装置I,锌片溶解,发生氧化反应,为原电池的负极,故B错误;
C.装置Ⅱ,负极为Zn-2e-=Zn2+,正极发生Cu2++2e-=Cu,电池总反应为:Zn+Cu2+═Zn2++Cu,故C正确;
D.装置Ⅱ,锌为负极,铜为正极,外电路中,电子从锌电极流向铜电极,故D错误.
故选C.
B.装置I,锌片溶解,发生氧化反应,为原电池的负极,故B错误;
C.装置Ⅱ,负极为Zn-2e-=Zn2+,正极发生Cu2++2e-=Cu,电池总反应为:Zn+Cu2+═Zn2++Cu,故C正确;
D.装置Ⅱ,锌为负极,铜为正极,外电路中,电子从锌电极流向铜电极,故D错误.
故选C.
点评:本题考查原电池知识,侧重于学生分析能力和基本理论的理解和运用的考查,注意把握金属的活泼性强弱以及电极方程式的书写,难度不大.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
把0.02mol/L CH3COOH溶液和0.01mol/L NaOH溶液以等体积混和,则混合液中微粒浓度关系正确的为( )
| A、c(CH3COO-)<c(Na+) |
| B、c(OH-)>c(H+) |
| C、c(CH3COOH)>c(CH3COO-) |
| D、c(CH3COOH)+c (CH3COO-)=0.01mol/L |
除去镁粉中混有的少量铝粉,可选用的试剂是( )
| A、稀盐酸 | B、稀硫酸 |
| C、氢氧化钠溶液 | D、氨水 |
100mL 6mol?L-1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量:①Na2CO3(s) ②BaCl2(aq) ③KNO3(aq) ④CH3COONa固体 ⑤NaCl(aq),其中组合正确的是( )
| A、①②③ | B、②④⑤ |
| C、③④⑤ | D、①③④ |
下列离子在溶液中能大量共存,加入(NH4)2Fe(SO4)2?6H2O晶体后,仍能大量共存的是( )
| A、Na+、H+、Cl-、NO3- |
| B、Na+、Mg2+、Cl-、SO42- |
| C、K+、Ba2+、OH-、I- |
| D、Cu2+、CO32-、Br-、ClO- |
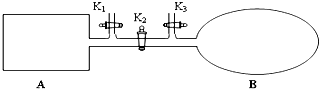 如图所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2,将各1mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L.
如图所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2,将各1mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L.