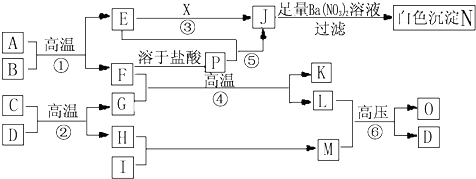
下列实验方案可行的是( )
| A、在淀粉溶液中加稀硫酸充分反应后,再加入银氨溶液,可检验淀粉的水解产物 |
| B、用溴水可以鉴别苯、乙醇、四氯化碳三种液体 |
| C、除去苯中的苯酚,可加入NaOH溶液后再分液 |
| D、将氯乙烷与NaOH的乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中,溶液褪色,证明氯乙烷发生了消去反应. |
某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50mL b mol?L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物).下列说法正确的是( )
| A、若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解 | ||
| B、若金属全部溶解,则溶液中一定含有Fe3+ | ||
| C、若金属全部溶解,且产生336mL气体(标准状况),则b=0.3 | ||
D、当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b<80y(1-
|
 甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )
甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )| A、若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物 |
| B、若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙可能为Na2O2 |
| C、若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序一定为:甲<丙<戊 |
| D、若丙、丁混合产生白烟,且丙分子为18电子分子,丁分子为10电子分子,则乙的水溶液可能具有漂白作用 |
下列化学实验基本操作中,正确的是( )
| A、配制溶液时,将量筒中液体倒入烧杯后,应将量筒洗涤,将洗涤液也倒入烧杯 |
| B、用干燥的pH试纸分别测1mol?L-1的NaOH溶液和1mol?L-1的H2SO4的pH |
| C、稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的烧杯中并不断搅拌 |
| D、向酒精灯加酒精时,应将试剂瓶中的酒精直接倒入酒精灯中 |
下列有关实验原理或操作正确的是( )
A、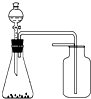 选择合适的试剂,装置可分别制取少量CO2、NO和O2 |
B、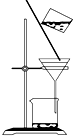 洗涤沉淀时(如图),向漏斗中加适量水,搅拌并滤干 |
| C、制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸 |
| D、用广泛pH试纸测得0.10 mol?L-1 NH4Cl溶液的pH=5.2 |
下列说法正确的是( )
| A、可用碘水鉴别苯、四氯化碳、乙醇三种无色液体 |
| B、取0.2mol NaCl固体于烧杯中,加入200 mL蒸馏水充分搅拌可配成1mol/L的NaCl溶液 |
| C、测定溶液的酸碱性时,应先将pH试纸润湿,然后进行检测 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等 |
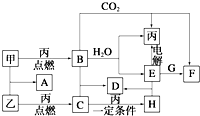 甲、乙、丙为常见单质.A、B、C、D、E、F、G、H均为中学化学中常见的化合物,其中B、G的焰色反应均为黄色,C能使品红溶液褪色.在一定条件下,各物质相互转化关系如图所示.请回答下列问题:
甲、乙、丙为常见单质.A、B、C、D、E、F、G、H均为中学化学中常见的化合物,其中B、G的焰色反应均为黄色,C能使品红溶液褪色.在一定条件下,各物质相互转化关系如图所示.请回答下列问题: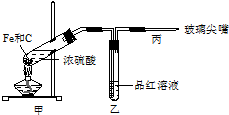 (1)下列仪器在使用前必须检查其是否漏水的是
(1)下列仪器在使用前必须检查其是否漏水的是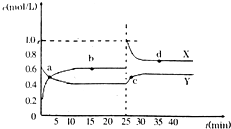 有关元素A、B、C、D的信息如下:
有关元素A、B、C、D的信息如下: