题目内容
下列化学实验基本操作中,正确的是( )
| A、配制溶液时,将量筒中液体倒入烧杯后,应将量筒洗涤,将洗涤液也倒入烧杯 |
| B、用干燥的pH试纸分别测1mol?L-1的NaOH溶液和1mol?L-1的H2SO4的pH |
| C、稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的烧杯中并不断搅拌 |
| D、向酒精灯加酒精时,应将试剂瓶中的酒精直接倒入酒精灯中 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.使用量筒时不需要洗涤量筒;
B.1mol?L-1的H2SO4氢离子浓度是2mol?L-1;
C.稀释浓硫酸时要将浓硫酸倒入水中,并用玻璃棒不断搅拌;
D.应用漏斗向酒精灯里添加酒精.
B.1mol?L-1的H2SO4氢离子浓度是2mol?L-1;
C.稀释浓硫酸时要将浓硫酸倒入水中,并用玻璃棒不断搅拌;
D.应用漏斗向酒精灯里添加酒精.
解答:
解:A.量筒使用错误,使用量筒时不需要洗涤量筒,若洗涤量筒并将洗涤液倒入烧杯,n值偏高,c偏高,故A错误;
B.1mol?L-1的H2SO4氢离子浓度是2mol?L-1,pH试纸无法测出,故B错误;
C.浓硫酸溶于水会放出大量的热,稀释浓硫酸时要将浓硫酸倒入水中,并用玻璃棒不断搅拌,不能将水倒入浓硫酸中,故C正确;
D.用漏斗向酒精灯里添加酒精,需要使用玻璃棒引流,漏斗的颈要紧靠在酒精内壁上,故D错误.
故选C.
B.1mol?L-1的H2SO4氢离子浓度是2mol?L-1,pH试纸无法测出,故B错误;
C.浓硫酸溶于水会放出大量的热,稀释浓硫酸时要将浓硫酸倒入水中,并用玻璃棒不断搅拌,不能将水倒入浓硫酸中,故C正确;
D.用漏斗向酒精灯里添加酒精,需要使用玻璃棒引流,漏斗的颈要紧靠在酒精内壁上,故D错误.
故选C.
点评:本题考查化学实验方案的评价,为高频考点,涉及溶液配制、pH试纸使用、浓硫酸的稀释及添加酒精等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
已知某元素的前8个电离能(I1/kJ?mol-1):I1=577,I2=1820,I3=2740,I4=11600,I5=14800,I6=18400,I7=23400,I8=27500.该元素原子的最外层有几个电子?( )
| A、1个 | B、2个 | C、3个 | D、4个 |
下列与有机物相关的叙述正确的是( )
| A、CH4O与C2H6O一定互为同系物 |
| B、1mol C6H6(苯)中含有3mol碳碳双键 |
| C、用浓硝酸与蛋白质的颜色反应鉴别部分蛋白质 |
| D、向乙酸乙酯中加入NaOH 溶液,振荡,分液分离除去乙酸乙酯中的少量乙酸 |
下列实验方案可行的是( )
| A、在淀粉溶液中加稀硫酸充分反应后,再加入银氨溶液,可检验淀粉的水解产物 |
| B、用溴水可以鉴别苯、乙醇、四氯化碳三种液体 |
| C、除去苯中的苯酚,可加入NaOH溶液后再分液 |
| D、将氯乙烷与NaOH的乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中,溶液褪色,证明氯乙烷发生了消去反应. |
下列有关生产、生活中的叙述正确的是( )
| A、煤经过气化和液化两个物理变化,可变为清洁能源 |
| B、古代的陶瓷、砖瓦,现代的有机玻璃、水泥都是硅酸盐产品 |
| C、明矾可用于水的消毒、杀菌:碳酸钡可用于钡餐透视 |
| D、单晶硅太阳能电池板可以将太阳能直接转变为电能 |
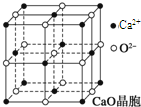 可以由下列反应合成三聚氰胺:CaO+3C
可以由下列反应合成三聚氰胺:CaO+3C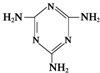 俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸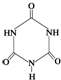 后,三聚氰酸与三聚氰胺分子相互之间通过
后,三聚氰酸与三聚氰胺分子相互之间通过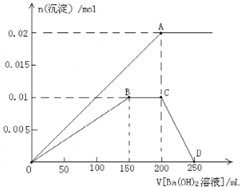 FeCl3在铜版印刷中用作印刷电路铜板腐蚀剂,按要求回答下列问题:
FeCl3在铜版印刷中用作印刷电路铜板腐蚀剂,按要求回答下列问题: