碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s).下列说法错误的是( )
| A、电池工作时,锌失去电子 |
| B、若电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-=Mn2O(s)+2OH-(aq),电池工作时,正极附近pH增大 |
| C、电池工作时,电子由正极通过外电路流向负极 |
| D、外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
将适量的MO2粉末投入热水中,一边搅拌,一边通入SO2气体,结果得到白色不溶物X,已知X既是氧化产物又是还原产物.下列判断错误的是( )
①MO2具有氧化性②白色不溶物X为MSO2③白色不溶物X为MSO4④白色不溶物X为MS.
①MO2具有氧化性②白色不溶物X为MSO2③白色不溶物X为MSO4④白色不溶物X为MS.
| A、①② | B、③④ | C、②④ | D、①③ |
有Fe2+、NO3-、Fe3+、NH4+、H2O和H+六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述错误的是( )
| A、氧化剂与还原剂的物质的量之比为1:8 |
| B、若有1mol NO3-被还原,转移8 mol e- |
| C、还原产物为NH4+ |
| D、若把该反应设计为原电池,则正极反应为Fe2+-e-=Fe3+ |
下列反应不属于氧化还原反应的是( )
| A、锌放入稀硫酸中 |
| B、高锰酸钾分解 |
| C、实验室制备氨气 |
| D、碳和水蒸气在高温下反应 |
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池反应为:FePO4+Li
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和锂,含Li+导电固体为电解质.下列有关LiFePO4电池说法正确的是( )
| 放电 |
| 充电 |
| A、可加入硫酸以提高电解质的导电性 |
| B、放电时电池内部Li+向负极移动. |
| C、充电过程中,电池正极材料的质量不变 |
| D、放电时电池正极反应为:FePO4+Li++e-=LiFePO4 |
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、pH=1的溶液中:Na+、K+、MnO4-、C2O42- |
| B、0.1mol/LFeCl3溶液中:Mg2+、NH4+、SCN-、SO42- |
| C、0.1mol/LNH4HCO3溶液中:K+、Na+、NO3-、Cl- |
| D、水电离出来的c(H+)=1×10-13mol/L的溶液中:Fe2+、Cu2+、SO42-、NO3- |
在强酸性溶液中下列离子能大量共存的是( )
| A、Ca2+、Na+、OH-、CO32- |
| B、Ag+、SO42-、HCO3-、Cl- |
| C、Cu2+、Na+、SO42-、NO3- |
| D、NH4+、S2-、Mg2+、Cu2+ |
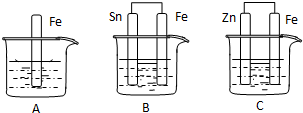 如图所示,烧杯中都盛有稀硫酸.
如图所示,烧杯中都盛有稀硫酸.