某主族元素原子的第一、二、三、四各级电离能依次为:899KJ/mol、1757KJ/mol、14840KJ/mol、18025KJ/mol,试分析该元素所在的族序数为( )
| A、IA族 | B、ⅡA族 |
| C、ⅢA族 | D、IVA族 |
在下面的电子结构中,第一电离能最小的原子可能是( )
| A、ns2np3 |
| B、ns2np5 |
| C、ns1 |
| D、ns2np6 |
(1)P和S (2)Mg和Ca (3)Al和Si三组原子中,分别找出第一电离能较高的原子,这三种原子的原子序数之和是( )
| A、40 | B、48 | C、41 | D、49 |
已知:五种(1~20号)元素的部分电离能数据(单位:kJ?mol-1),
推测上述五种元素,处于周期表中同一族的是( )
| 元素代号 | I1 | I2 | I3 | I4 |
| X | 2080 | 4000 | 6100 | 9400 |
| Y | 500 | 4600 | 6900 | 9500 |
| Z | 740 | 1500 | 7700 | 10500 |
| M | 580 | 1800 | 2700 | 11600 |
| N | 420 | 4100 | 6400 | 8900 |
| A、X和Y | B、Y和N |
| C、M和N | D、Y和M |
X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知( )
| A、X的原子半径大于Y的原子半径 |
| B、X的电负性小于Y的电负性 |
| C、X的阴离子半径大于Y的阳离子半径 |
| D、X的I1小于Y 的I1 |
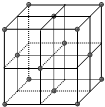 碳有多种同素异形体,常见的有金刚石,石墨,和C60(足球烯)分子,根据报道科研人员应用计算机模拟出结构类似C60的物质N60分子和Si60分子,
碳有多种同素异形体,常见的有金刚石,石墨,和C60(足球烯)分子,根据报道科研人员应用计算机模拟出结构类似C60的物质N60分子和Si60分子,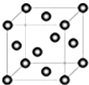 含有NaOH的Cu(OH)2悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米Cu2O.
含有NaOH的Cu(OH)2悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米Cu2O.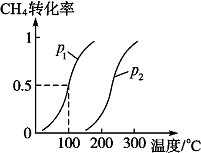 将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应Ⅱ:CH4(g)+H2O(g)?CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图.
将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应Ⅱ:CH4(g)+H2O(g)?CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图.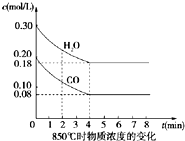 在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生以下反应:
在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生以下反应: