下列说法中正确的是( )
| A、饮用水可以用明矾、漂白粉来净化,两者的作用原理相同 |
| B、常温常压下,78gNa2O2固体中所含阴离子数一定为NA |
| C、NH4Cl、MgCl2均为离子化合物,均含有离子键和共价键 |
| D、实验室中浓硝酸保存在带橡胶塞的棕色细口试剂瓶中 |
下列化合物中,既含有离子键又含有共价键的是( )
| A、BaCl2 |
| B、H2O |
| C、Ca(OH)2 |
| D、Na2O |
将体积为1mL,浓度为0.5mol/L的乙酸和体积为2mL,浓度为0.25mol/L的NaOH溶液混和,所得溶液中离子浓度由大到小的顺序是( )
| A、c(Na+)>c(CH3COO-)>c (OH-)>c(H+) |
| B、c(Na+)=c(CH3COO-),c(CH3COO-)>c (OH-)>c(H+) |
| C、c(Na+)>c (OH-)>c(CH3COO-)>c(H+) |
| D、c(Na+)>c (OH-)>c(H+)>c(CH3COO-) |
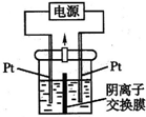 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO3-+5I-+3H2O.下列说法不正确的是( )
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO3-+5I-+3H2O.下列说法不正确的是( )| A、右侧发生的电极方程式:2H2O+2e-=H2↑+2OH- | ||||
| B、电解结束时,右侧溶液中含有IO3- | ||||
C、电解槽内发生反应的总化学方程式KI+3H2O
| ||||
| D、如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变 |
下列物质中,只含离子键的是( )
| A、NH4Cl |
| B、CaCl2 |
| C、HCl |
| D、NaOH |
下列叙述中正确的是( )
| A、常温下,10mlpH=12的氢氧化钠溶液中加入10mlpH=2的HA,所得溶液pH≤7 |
| B、25℃时,0.1mol/L与0.01mol/L的氯化铵溶液的pH前者大 |
| C、室温时浓度均为0.1mol/L的NH3?H2O和NH4Cl的混合液,pH为10,则,c(NH4+)+c(H+)<c(NH3?H2O)+c(OH-) |
| D、0.1mol/LNa2S溶液:c(Na+)>c(S2-)>c(HS-)>c(OH-)>c(H+) |
化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A、太阳能电池板中的硅,在元素周期表中处于金属与非金属的交界位置 |
| B、煤的气化或液化技术,可以降低污染 |
| C、镁粉可用来作信号弹和烟花,氧化镁可制作耐高温材料 |
| D、NaHCO3能与碱反应,因此食品工业用小苏打做焙制糕点的膨松剂 |
已知HCN的电离常数Ka=5×10-10,H2CO3离常数Ka1=4.3×10-7、Ka2=5.6×10-11,判断在等浓度的NaCN、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A、c(HCO3-)>c(CN- )>c(OH- ) |
| B、c(CN- )>c(HCO3-)>c(H+ ) |
| C、c(HCN)+c(CN- )=c(HCO3-)+c(H2CO3) |
| D、c(Na+ )+c(H+ )=c(HCO3- )+c(CN- )+C(OH- ) |
下列陈述ⅠⅡ正确并且有因果关系的是( )
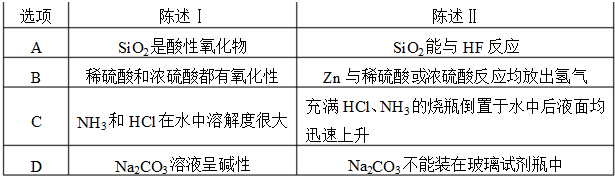

| A、A | B、B | C、C | D、D |
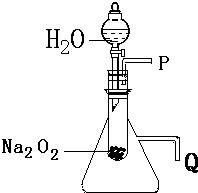 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.