下列图标是国家节水标志的是( )
A、 |
B、 |
C、 |
D、 |
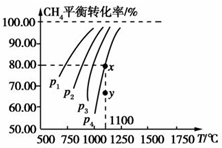 在2L的恒容密闭容器中,充入0.2molCO2和0.2molCH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )
在2L的恒容密闭容器中,充入0.2molCO2和0.2molCH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )| A、上述反应的△H>0 |
| B、压强:P4>P3>P2>P1 |
| C、1100℃,P1时该反应平衡常数约为16.4 |
| D、压强为p4时,在y点:V正>V逆 |
下列实验中,(1)配制一定物质的量浓度的溶液(2)pH试纸的使用(3)过滤(4)蒸发,均需用到的仪器是( )
| A、试管 | B、容量瓶 |
| C、玻璃棒 | D、漏斗 |
 下列说法中正确的是( )
下列说法中正确的是( )| A、Na2S2O3+2HCl?2NaCl+S↓+SO2↑+H2O在加热条件下化学反应速率增大的主要原因是该反应是吸热反应,加热使平衡向正反应方向移动 |
| B、若在恒容容器中发生反应:N2+3H2?2NH3,达到平衡后再充入适量NH3,由于压强增大,化学平衡向正反应方向移动 |
| C、在合成氨反应中,其他条件相同时,在有催化剂时(a)和无催化剂时(b)的速率-时间图象可用图一表示 |
| D、若在恒压容器中发生反应:2SO3?2SO2+O2,达到平衡后再充入适量He,其速率-时间图象可用图二表示 |
要配制浓度为2mol?L-1NaOH溶液100mL,下面的操作正确的是( )
| A、称取8gNaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 |
| B、称取8gNaOH固体,放入100mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL |
| C、称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀. |
| D、用100mL量筒量取40mL5mol?L-1NaOH溶液,倒入烧杯中,加水搅拌,将溶液转移至100mL容量瓶中,洗涤烧杯和玻璃棒并转移洗涤液,再加水至刻度,摇匀. |
 某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据,下列有关说法错误的是( )
某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据,下列有关说法错误的是( )| A、该反应的化学方程式为3X+Y═2Z |
| B、2 min时,反应达最大限度,但化学反应仍在进行 |
| C、反应开始至2 min,Z的反应速率为0.10 mol?L-1?min-1 |
| D、反应达到平衡时,压强是开始时的0.9倍 |
下列实验操作中和事故、药品的处理中正确的是( )
| A、“粗盐提纯“的实验中,当蒸发皿中出现较多固体时,停止加热 |
| B、少量浓硫酸沾在皮肤上立即用氢氧化钠冲洗 |
| C、有腐蚀性D的药品直接放在天平托盘上称重 |
| D、提取溴水中的溴时,可以选择酒精灯、作萃取剂 |
 向绝热恒容密闭容器中只通入A(g)和B(g),在一定条件下使反应A(g)+B(g)?C(g)+D(g)达到平衡,反应过程中正反应速率随时间变化的示意图如图所示.下列说法正确的是( )
向绝热恒容密闭容器中只通入A(g)和B(g),在一定条件下使反应A(g)+B(g)?C(g)+D(g)达到平衡,反应过程中正反应速率随时间变化的示意图如图所示.下列说法正确的是( )| A、该反应正反应为吸热反应 |
| B、反应物的浓度:a点小于b点 |
| C、反应在c点达到平衡 |
| D、反应达到平衡时,升高温度,逆反应速率将增大 |
已知:将Cl2通入适量KOH溶液,产物中可能有KC1、KClO、KClO3,且
的值与温度高低有关.当n(KOH)=a mol时,下列有关说法错误的是( )
| c(Cl-) |
| c(ClO-) |
A、参加反应的氯气的物质的量等于
| ||||||||
B、若某温度下,反应后
| ||||||||
C、改变温度,产物中KC1O3的最大理论产量为
| ||||||||
D、改变温度,反应中转移电子的物质的量ne的范围:
|