0 130994 131002 131008 131012 131018 131020 131024 131030 131032 131038 131044 131048 131050 131054 131060 131062 131068 131072 131074 131078 131080 131084 131086 131088 131089 131090 131092 131093 131094 131096 131098 131102 131104 131108 131110 131114 131120 131122 131128 131132 131134 131138 131144 131150 131152 131158 131162 131164 131170 131174 131180 131188 203614

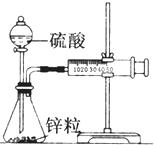 某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.
某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.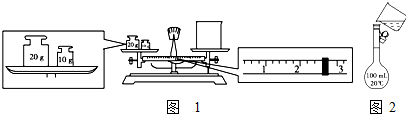
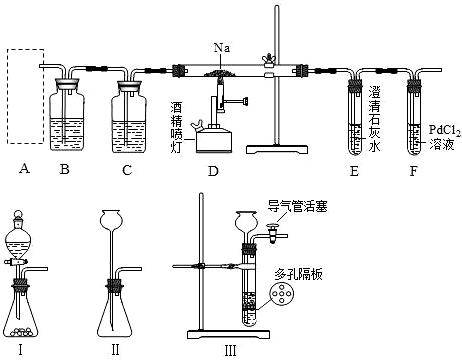
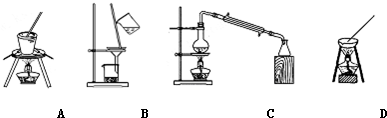
 如图是甲同学设计的证明CO具有还原性的实验装置.回答下列问题:
如图是甲同学设计的证明CO具有还原性的实验装置.回答下列问题: