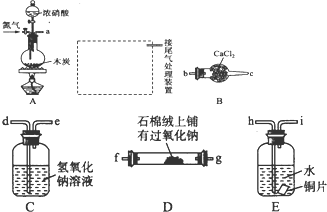
题目内容
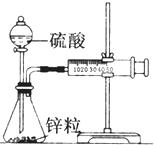 某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.
某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.【实验目的】测量锌和稀硫酸反应的速率
【实验用品】锥形瓶、双孔塞、分液漏斗、直角导管、50mL注射器、铁架台、秒表、锌粒、1mol?L-1的H2SO4、4mol?L-1的H2SO4.
【实验步骤】
(1)甲同学取一套如图装置,加入40mL 1mol?L-1的H2SO4,测量收集10mL H2所需的时间.
(2)乙同学取另一套同样的装置,加入40mL 4mol?L-1的H2SO4,测量收集10mL H2所需的时间.
回答下列问题:
(1)Zn与稀H2SO4反应的离子方程式为
(2)收集10mL H2所需时间:甲
(3)下列说法正确的是
A.本实验中甲、乙两同学所用锌粒的表面积要相同
B.装置气密性要好
C.40mL的H2SO4要迅速加入
D.收集气体还可以用排水法收集
E.若用98%的浓H2SO4,则反应最快.
考点:测定某些化学反应的速率
专题:化学反应速率专题
分析:(1)金属锌可以和硫酸反应生成硫酸锌和氢气,据此书写离子方程式;
(2)浓度越大,反应速率越快,反应产生等量的气体需要的时间越短;
(3)A.研究浓度对反应速率的影响,本实验中所用锌粒的表面积要相同,根据控制变量法来回答;
B.根据测量收集10mL H2所需的时间,要求生成的氢气体积测定必须准确;
C.40mL的H2SO4要迅速加入,防止气体的体积测定误差的出现;
D.氢气的收集可以用排水法收集
E.若用98%的浓H2SO4,金属和浓硫酸的反应产物是二氧化硫,不是氢气.
(2)浓度越大,反应速率越快,反应产生等量的气体需要的时间越短;
(3)A.研究浓度对反应速率的影响,本实验中所用锌粒的表面积要相同,根据控制变量法来回答;
B.根据测量收集10mL H2所需的时间,要求生成的氢气体积测定必须准确;
C.40mL的H2SO4要迅速加入,防止气体的体积测定误差的出现;
D.氢气的收集可以用排水法收集
E.若用98%的浓H2SO4,金属和浓硫酸的反应产物是二氧化硫,不是氢气.
解答:
解:(1)金属锌可以和硫酸反应生成硫酸锌和氢气,离子方程式为:Zn+2H+=Zn2++H2↑,故答案为:Zn+2H+=Zn2++H2↑;
(2)1mol?L-1的H2SO4浓度小于4mol?L-1的H2SO4的,浓度越大,反应速率越快,反应产生等量的气体需要的时间越短,故答案为:大于;小于;
(3)A.研究浓度对反应速率的影响,本实验中所用锌粒的表面积要相同,故A正确;
B.根据测量收集10mL H2所需的时间,要求生成的氢气体积测定必须准确,气密性必须好,故B正确;
C.40mL的H2SO4要迅速加入,防止气体的体积测定误差的出现,故C正确;
D.氢气不溶于水,收集可以用排水法收集,故D正确;
E.若用98%的浓H2SO4,金属和浓硫酸的反应产物是二氧化硫,不是氢气,故E错误.
故选ABCD.
(2)1mol?L-1的H2SO4浓度小于4mol?L-1的H2SO4的,浓度越大,反应速率越快,反应产生等量的气体需要的时间越短,故答案为:大于;小于;
(3)A.研究浓度对反应速率的影响,本实验中所用锌粒的表面积要相同,故A正确;
B.根据测量收集10mL H2所需的时间,要求生成的氢气体积测定必须准确,气密性必须好,故B正确;
C.40mL的H2SO4要迅速加入,防止气体的体积测定误差的出现,故C正确;
D.氢气不溶于水,收集可以用排水法收集,故D正确;
E.若用98%的浓H2SO4,金属和浓硫酸的反应产物是二氧化硫,不是氢气,故E错误.
故选ABCD.
点评:本题涉及影响化学反应速率的因素知识,注意知识的迁移和应用是关键,难度不大.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案
相关题目
下列水解的离子方程式正确的是( )
| A、S2-+2H2O?H2S+2OH- |
| B、Fe3++3H2O?Fe(OH)3+3H+ |
| C、HCO3-+H2O?CO32-+H3O+ |
| D、HS-+H2O?H2S↑+OH- |
下列化学用语表达正确的是( )
A、S2-的结构示意图: |
B、NaCl的电子式: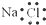 |
| C、Cl2的结构式:Cl-Cl |
| D、NaHCO3的电离方程式:NaHCO3=Na++H++CO32- |
 某课题组为探究淡黄色草酸亚铁晶体(FeC2O4?2H2O)的化学性质,进行了一系列实验探究.
某课题组为探究淡黄色草酸亚铁晶体(FeC2O4?2H2O)的化学性质,进行了一系列实验探究.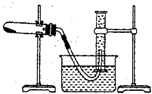
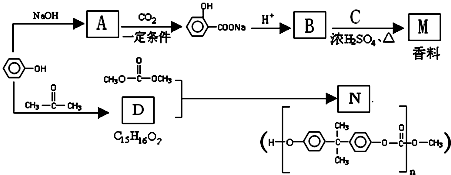
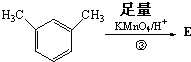 ,则E的分子式为
,则E的分子式为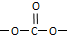 结构在上述同分异构体中,有一类有机物分子中苯环上只有2个取代基,写出其中任一种与足量NaOH溶液共热反应的化学方程式
结构在上述同分异构体中,有一类有机物分子中苯环上只有2个取代基,写出其中任一种与足量NaOH溶液共热反应的化学方程式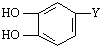 ,其中取代基-Y中不含支链,含有碳碳双键,咖啡酸有如下转化关系:
,其中取代基-Y中不含支链,含有碳碳双键,咖啡酸有如下转化关系:
 ,试写出D的属于芳香醇的其中2种同分异构体是
,试写出D的属于芳香醇的其中2种同分异构体是