题目内容
某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去).已知:常温下,CO能使一些化合物中的金属离子还原
例如:PdCl2+CO+H2O=Pd↓+CO2+2HCl.反应生成黑色的金属钯,此反应也可用来检测微量CO的存在.
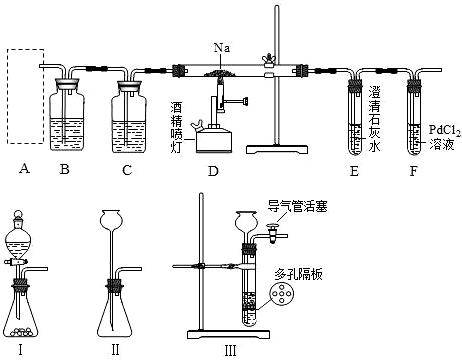
请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是 ,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是 (填写“Ⅰ”、“Ⅱ”或“Ⅲ”).若要制取干燥、纯净的CO2气体,装置B、C中各盛放的试剂分别为 、 .
(2)装入药品后,在点燃酒精喷灯前,必须进行的操作是 .待装置 (填写字母)中出现 现象时,再点燃酒精喷灯,这步操作的目的是 .
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是 .
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式(需注明正确的反应条件)是 .
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐还是酸式盐 理由: .
例如:PdCl2+CO+H2O=Pd↓+CO2+2HCl.反应生成黑色的金属钯,此反应也可用来检测微量CO的存在.

请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是
(2)装入药品后,在点燃酒精喷灯前,必须进行的操作是
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式(需注明正确的反应条件)是
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐还是酸式盐
考点:性质实验方案的设计
专题:实验设计题
分析:(1)实验室常用碳酸钙与稀盐酸反应制取二氧化碳,制取气体的装置能“随开随用,随关随停”,是利用的启普发生器原理分析选择装置,制得的二氧化碳中含有氯化氢和水蒸气,利用装置B除氯化氢,利用装置C除水蒸气;
(2)为避免空气的影响,实验前先通二氧化碳充满装置后,再点燃酒精喷灯;
(3)①装置F中无明显现象,证明没有CO生成,装置D中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,其中一种固体为碳酸钠,另一种固体为C;
②装置D中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,装置F中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应产物为碳酸钠和CO;
(4)根据反应物的成分和质量守恒解答.
(2)为避免空气的影响,实验前先通二氧化碳充满装置后,再点燃酒精喷灯;
(3)①装置F中无明显现象,证明没有CO生成,装置D中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,其中一种固体为碳酸钠,另一种固体为C;
②装置D中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,装置F中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应产物为碳酸钠和CO;
(4)根据反应物的成分和质量守恒解答.
解答:
解:(1)实验室常用碳酸钙与稀盐酸反应制取二氧化碳,反应方程式为:CaCO3+2H+=Ca2++H2O+CO2↑;制取气体的装置能“随开随用,随关随停”,是利用的启普发生器原理分析选择装置;制得的二氧化碳中含有氯化氢和水蒸气,利用装置B饱和NaHCO3除氯化氢,利用装置C浓H2SO4除水蒸气;
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;Ⅲ;饱和NaHCO3;浓H2SO4;
(2)为了避免空气中氧气、水蒸气影响探究二氧化碳和钠反应的产物分析,需要先把装置中空气排出,所以打开Ⅲ的导气管活塞,先通一会CO2气体,使装置充满二氧化碳气体后再点燃酒精喷灯;
故答案为:打开Ⅲ的导气管活塞,先通一会CO2气体;E;浑浊;排出该装置中的空气,避免空气中氧气、水蒸气影响探究二氧化碳和钠反应;
(3)①装置F中无明显现象,证明没有CO生成,装置D中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,
其中一种固体为碳酸钠,另一种固体为C,反应的方程式为4Na+3CO2
2Na2CO3+C;
故答案为:4Na+3CO2
2Na2CO3+C;
②由题意可知,装置D中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,
装置F中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应产物为碳酸钠和CO,反应的化学方程式为2Na+2CO2
Na2CO3+CO;
故答案为:2Na+2CO2
Na2CO3+CO;
(4)根据质量守恒定律可知,反应物CO2和Na中共有三种元素,没有氢元素,因此不能生成酸式盐,只能生成正盐;
故答案为:生成正盐;因为根据质量守恒定律可知,反应物共有三种元素,没有氢元素,因此不能生成酸式盐.
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;Ⅲ;饱和NaHCO3;浓H2SO4;
(2)为了避免空气中氧气、水蒸气影响探究二氧化碳和钠反应的产物分析,需要先把装置中空气排出,所以打开Ⅲ的导气管活塞,先通一会CO2气体,使装置充满二氧化碳气体后再点燃酒精喷灯;
故答案为:打开Ⅲ的导气管活塞,先通一会CO2气体;E;浑浊;排出该装置中的空气,避免空气中氧气、水蒸气影响探究二氧化碳和钠反应;
(3)①装置F中无明显现象,证明没有CO生成,装置D中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,
其中一种固体为碳酸钠,另一种固体为C,反应的方程式为4Na+3CO2
| ||
故答案为:4Na+3CO2
| ||
②由题意可知,装置D中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,
装置F中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应产物为碳酸钠和CO,反应的化学方程式为2Na+2CO2
| ||
故答案为:2Na+2CO2
| ||
(4)根据质量守恒定律可知,反应物CO2和Na中共有三种元素,没有氢元素,因此不能生成酸式盐,只能生成正盐;
故答案为:生成正盐;因为根据质量守恒定律可知,反应物共有三种元素,没有氢元素,因此不能生成酸式盐.
点评:本题考查了实验装置的选择,物质性质的实验设计验证分析应用,主要是钠及其化合物性质的判断理解,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
用NA代表阿伏伽德罗常数,下列说法正确的是( )
| A、标准状况下,2.24LCHCl3的分子数0.1NA |
| B、1molNH3中含有3NA对电子对 |
| C、9.2gNO2和N2O4的混合气中含有的氮原子数为大于0.2NA |
| D、VL a mol?L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
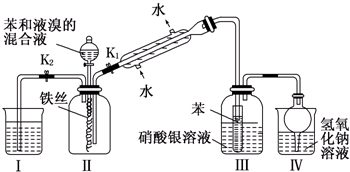
 为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
 如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.
如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容. 你认为该同学的错误步骤有
你认为该同学的错误步骤有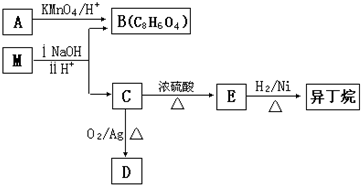 苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p-xylene,缩写为PX)是化学工业的重要原料.
苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p-xylene,缩写为PX)是化学工业的重要原料.