已知室温时,0.1mol/L某一元酸HA,PH=4,下列说法正确的是( )
| A、HA在水中有0.001%发生电离 |
| B、HA的电离平衡常数K=10-8mol/L |
| C、升高温度时,PH增大 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列有关制取蒸馏水的装置和操作的说法中,不正确的是( )
| A、温度计的水银球应插入蒸馏烧瓶内的自来水中 |
| B、冷凝管内水的流向是下进上出 |
| C、实验中需在自来水中加几片碎瓷片 |
| D、蒸馏烧瓶底部必须垫石棉网 |
如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是( )
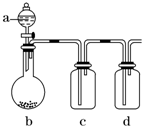

| A、若a为浓硫酸,b为Na2SO3固体,c中盛石蕊溶液,则c中溶液先变红后褪色 |
| B、若a为浓盐酸,b为MnO2,c中盛品红溶液,则c中溶液不褪色 |
| C、若a为醋酸溶液,b为贝壳,c中盛过量澄清石灰水,则c中溶液变浑浊 |
| D、若a为浓氨水,b为生石灰,c中盛AlCl3溶液,则c中产生白色沉淀 |
下列实验装置能达到相应实验目的是( )
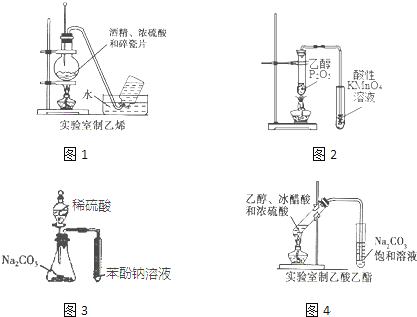

| A、图1装置一定可以制得乙烯 |
| B、图2装置可以证明CH3CH2OH发生消去反应生成了乙烯 |
| C、图3所示装置可以证明碳酸酸性强于苯酚 |
| D、实验室常用图4所示装置制取少量的乙酸乙酯 (夹持物略) |
常温下,Ksp(CaCO3)=4.96×10-9,Ksp(MgCO3)=6.82×10-6.含有MgCO3沉淀的MgCl2溶液中,已知c(Mg2+)=0.2mol/L.如果加入等体积的CaCl2溶液,若要产生CaCO3沉淀,加入CaCl2溶液的物质的量浓度最小约为( )
| A、7.27×10-5mol/L |
| B、1.45×10-4mol/L |
| C、2.9×10-4mol/L |
| D、5.8×10-4mol/L |
下列实验可以达到预期实验目的是( )
| A、实验内容:将木炭与浓硫酸共热,得到的气体通入澄清石灰水.实验目的:检验木炭的氧化产物是CO2. |
| B、实验内容:加入足量铁屑,充分反应后,过滤.实验目的:除去FeCl2溶液中的少量FeCl3. |
| C、实验内容:将1moLCuSO4?5H2O溶解在1L 水中.实验目的:制备1moL/L的CuSO4溶液 |
| D、实验内容:饱和氯化铁溶液中滴加氨水.实验目的:制备Fe(OH)3胶体 |
已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10.现向1L2mol/LHF溶液中加入1L 0.2mol/LCaCl2溶液,则下列说法中,正确的是( )
| A、25℃时,0.1 mol/LHF溶液中pH=1 |
| B、Ksp(CaF2)随温度和浓度的变化而变化 |
| C、该体系中没有沉淀产生 |
| D、该体系中HF与CaCl2反应产生沉淀 |
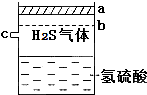 已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度…在密闭容器里盛有饱和H2S溶液和H2S气体,可上下移动的活塞停止在a处,如图所示.
已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度…在密闭容器里盛有饱和H2S溶液和H2S气体,可上下移动的活塞停止在a处,如图所示.