题目内容
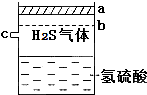 已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度…在密闭容器里盛有饱和H2S溶液和H2S气体,可上下移动的活塞停止在a处,如图所示.
已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度…在密闭容器里盛有饱和H2S溶液和H2S气体,可上下移动的活塞停止在a处,如图所示.(1)饱和H2S溶液中存在
(2)若将容器顶盖由a压到b位置,则H2S溶液中,各离子浓度的变化情况是
(3)若从c处不断通入过量的SO2气体,溶液中H+浓度将
A.不断增大 B.先减小,后增大到某值 C.不变 D.先增大,后减小到某值
(4)若由c处不断通入N2,则溶液中H+浓度将
考点:弱电解质在水溶液中的电离平衡
专题:
分析:(1)H2S水溶液中存在电离平衡H2S?H++HS-和HS-?H++S2-;
(2)若将容器顶盖由a压到b位置,增大压强,溶液中硫化氢的浓度变大,平衡H2S?H++HS-和HS-?H++S2-正向移动;
(3)硫化氢和二氧化硫反应生成硫和水,亚硫酸酸性大于氢硫酸;
(4)若由c处不断通入N2,氮虽是非反应气体,如果不断通入N2,体系温度升高,硫化氢的溶解度变小,H2S水溶液中存在电离平衡H2S?H++HS-和HS-?H++S2-逆向移动.
(2)若将容器顶盖由a压到b位置,增大压强,溶液中硫化氢的浓度变大,平衡H2S?H++HS-和HS-?H++S2-正向移动;
(3)硫化氢和二氧化硫反应生成硫和水,亚硫酸酸性大于氢硫酸;
(4)若由c处不断通入N2,氮虽是非反应气体,如果不断通入N2,体系温度升高,硫化氢的溶解度变小,H2S水溶液中存在电离平衡H2S?H++HS-和HS-?H++S2-逆向移动.
解答:
解:(1)H2S水溶液中存在电离平衡H2S?H++HS-、HS-?H++S2-和水的电离平衡,所以含有水分子、硫化氢分子、H+、HS-、S2-和OH-,故答案为:6;
(2)若将容器顶盖由a压到b位置,增大压强,溶液中硫化氢的浓度变大,平衡H2S?H++HS-和HS-?H++S2-正向移动,导致H+、HS-、S2-浓度变大,而氢离子与氢氧根离子的积是个定值,所以氢氧根离子浓度减小,故答案为:H+、HS-、S2-;OH-;
(3)SO2+2H2S=3S↓+2H2O,平衡向左移动,H2O+SO2=H2SO3,亚硫酸酸性大于氢硫酸,所以先减小,后增大到某值,故选:B;
(4)若由c处不断通入N2,氮虽是非反应气体,如果不断通入N2,体系温度升高,硫化氢的溶解度变小,H2S水溶液中存在电离平衡H2S?H++HS-和HS-?H++S2-逆向移动,所以氢离子的浓度减小,故答案为:变小.
(2)若将容器顶盖由a压到b位置,增大压强,溶液中硫化氢的浓度变大,平衡H2S?H++HS-和HS-?H++S2-正向移动,导致H+、HS-、S2-浓度变大,而氢离子与氢氧根离子的积是个定值,所以氢氧根离子浓度减小,故答案为:H+、HS-、S2-;OH-;
(3)SO2+2H2S=3S↓+2H2O,平衡向左移动,H2O+SO2=H2SO3,亚硫酸酸性大于氢硫酸,所以先减小,后增大到某值,故选:B;
(4)若由c处不断通入N2,氮虽是非反应气体,如果不断通入N2,体系温度升高,硫化氢的溶解度变小,H2S水溶液中存在电离平衡H2S?H++HS-和HS-?H++S2-逆向移动,所以氢离子的浓度减小,故答案为:变小.
点评:本题考查弱电解质的电离,明确离子间发生的反应是解本题关键,注意通入过量的SO2气体时,首先反应导致平衡移动,后来再通变为亚硫酸溶液,为易错点.

练习册系列答案
相关题目
已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10.现向1L2mol/LHF溶液中加入1L 0.2mol/LCaCl2溶液,则下列说法中,正确的是( )
| A、25℃时,0.1 mol/LHF溶液中pH=1 |
| B、Ksp(CaF2)随温度和浓度的变化而变化 |
| C、该体系中没有沉淀产生 |
| D、该体系中HF与CaCl2反应产生沉淀 |
除去括号内杂质所用试剂和方法不正确的是( )
| A、植物油(水)--分液 |
| B、Fe(OH)3胶体(HCl)--渗析 |
| C、水(NaCl)--蒸馏 |
| D、CO2(HCl)--氢氧化钠溶液,洗气 |
下列提纯方法不正确的是( )
| A、除去KNO3中的NaCl杂质----结晶.重结晶 |
| B、除去食盐中的泥沙-----过滤 |
| C、除去KCl中的K2CO3-----加适量盐酸 |
| D、除去碘水中的水-----升华 |
在一定条件下某反应的热化学方程式为:2SO2(g)+O2(g)?2SO3(g);△H=-197kJ/mol
现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如表所示.根据以下数据,下列叙述正确的是( )
现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如表所示.根据以下数据,下列叙述正确的是( )
| 容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |
| A、Q2=98.5 kJ |
| B、2SO2(g)+O2(g)?2SO3(s);△H>-197KJ/mol |
| C、丙容器中压强大于乙,所以丙的反应速率大于乙 |
| D、2Q3<Q1<197KJ |
下列说法正确的是( )
| A、HR溶液的导电性较弱,HR属于弱酸 |
| B、某化合物溶于水导电,则该化合物为电解质 |
| C、根据电解质在其水溶液中能否完全电离,将电解质分为强电解质和弱电解质 |
| D、食盐是电解质,食盐的水溶液也是电解质 |
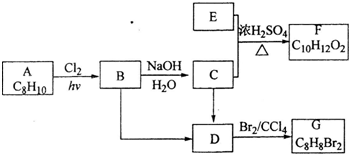
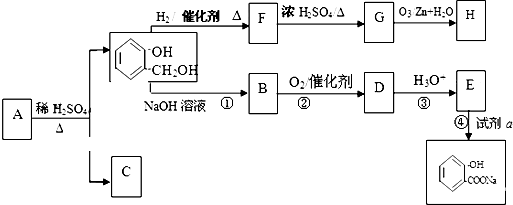
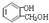 与饱和溴水反应的化学方程式
与饱和溴水反应的化学方程式 反应是否进行完全,设计一个简单实验加以证明并写出实验操作、现象及结论为
反应是否进行完全,设计一个简单实验加以证明并写出实验操作、现象及结论为