将铝、铁物质的量均为0.2mol的某种铝铁合金粉末分别于下列溶液充分反应(溶液均过量),放出氢气最多的是( )
| A、18.4mol?L-1H2SO4溶液 |
| B、1.5mol?L-1 HCl溶液 |
| C、4mol?L-1HNO3溶液 |
| D、3mol?L-1NaOH溶液 |
用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:下列叙述正确的是( )


| A、试剂X可以是盐酸 |
| B、反应①过滤后所得沉淀为氢氧化铁 |
| C、图中所示转化反应都不是氧化还原反应 |
| D、操作②中发生的化学方程式为NaAlO2+2H2O+CO2=Al(OH)3↓+NaHCO3 |
现将1mo1Cu2S与144克FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2、CuSO4的混合溶液,并产生NO气体.则最终消耗的硝酸的物质的量是( )
| A、12 mo1 |
| B、15 mo1 |
| C、16 mo1 |
| D、17 mo1 |
 某同学研究铝及其化合物的性质时设计了如下两个实验方案.
某同学研究铝及其化合物的性质时设计了如下两个实验方案.方案一:2.7g Al
| 100mL稀盐酸 |
| NaOH溶液 |
方案二:2.7g Al
| 100mLNaOH溶液 |
| 稀盐酸 |
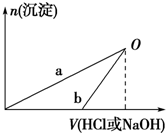
已知:NaOH溶液和稀盐酸的浓度均是3mol?L-1,如图是向X溶液和Y溶液中分别加入NaOH溶液和稀盐酸时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法正确的是( )
| A、在O点时两方案中所得溶液的溶质物质的量相等 |
| B、b曲线表示的是向X溶液中加入NaOH溶液 |
| C、X溶液溶质为AlCl3,Y溶液溶质为NaAlO2 |
| D、a、b曲线表示的反应都是氧化还原反应 |
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是( )
| A、过量新制的氯水滴到蓝色的石蕊试纸上,试纸先变红,说明氯水中含有H+ |
| B、向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
| C、向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| D、氯水能使有色花瓣褪色,说明氯水中含有Cl2 |
下列有关实验的说法正确的是( )
| A、除去铁粉中混有少量铝粉,可加入过量的稀硫酸溶液,完全反应后过滤 |
| B、为测定熔融氢氧化钠的导电性,不能在瓷坩埚中熔化氢氧化钠固体后进行测量 |
| C、制备Fe(OH)3胶体,通常是将NaOH溶液滴入FeCl3溶液中 |
| D、某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |