题目内容
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是( )
| A、过量新制的氯水滴到蓝色的石蕊试纸上,试纸先变红,说明氯水中含有H+ |
| B、向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
| C、向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| D、氯水能使有色花瓣褪色,说明氯水中含有Cl2 |
考点:探究氯水、氯气的漂白作用
专题:
分析:溶液中存在平衡Cl2+H2O?HCl+HClO,蓝色的石蕊试纸上,试纸先变红,说明溶液呈酸性,溶液中HCl与硝酸银反应产生AgCl白色沉淀,而溶液呈酸性,能与碳酸氢钠反应生成二氧化碳,溶液中HClO具有漂白性,能使有色花瓣褪色.
解答:
解:溶液中存在平衡Cl2+H2O?HCl+HClO,
A.过量新制的氯水滴到蓝色的石蕊试纸上,试纸先变红,说明溶液呈酸性,则氯水中含有H+,故A正确;
B.溶液与硝酸银反应产生白色沉淀,只能是氯离子与银离子反应得到AgCl白色沉淀,说明氯水中含有Cl-,故B正确;
C.溶液呈酸性,能与碳酸氢钠反应生成二氧化碳,故C正确;
D.溶液中氯气、HClO都强氧化性,但只有HClO体现漂白性,所以使有色花瓣褪色说明氯水中含有HClO不是氯气,故D错误,
故选D.
A.过量新制的氯水滴到蓝色的石蕊试纸上,试纸先变红,说明溶液呈酸性,则氯水中含有H+,故A正确;
B.溶液与硝酸银反应产生白色沉淀,只能是氯离子与银离子反应得到AgCl白色沉淀,说明氯水中含有Cl-,故B正确;
C.溶液呈酸性,能与碳酸氢钠反应生成二氧化碳,故C正确;
D.溶液中氯气、HClO都强氧化性,但只有HClO体现漂白性,所以使有色花瓣褪色说明氯水中含有HClO不是氯气,故D错误,
故选D.
点评:本题考查氯水的性质,难度不大,侧重对基础知识的考查,需要学生熟练掌握基础知识.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
实验室可用如图来制取的气体是( )
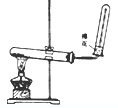

| A、氯气 | B、氧气 | C、氨气 | D、氢气 |
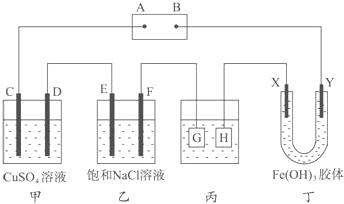
 +R
+R +R
+R