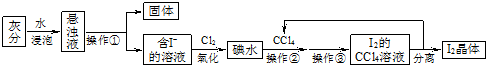
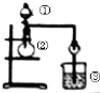
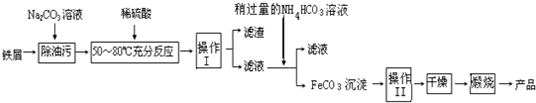
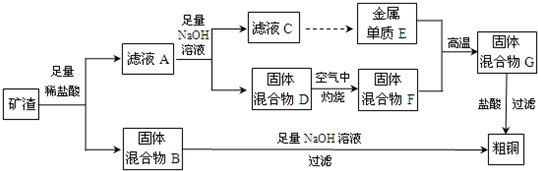
0 130809 130817 130823 130827 130833 130835 130839 130845 130847 130853 130859 130863 130865 130869 130875 130877 130883 130887 130889 130893 130895 130899 130901 130903 130904 130905 130907 130908 130909 130911 130913 130917 130919 130923 130925 130929 130935 130937 130943 130947 130949 130953 130959 130965 130967 130973 130977 130979 130985 130989 130995 131003 203614