乙醇和乙酸乙酯组成的混合物中,已知其中氧的质量分数为36%,则100g此混合物完全燃烧后生成水的质量为( )
| A、104g | B、90g |
| C、92g | D、88g |
下列有关除杂质(括号中为杂质)的操作中,错误的是( )
| A、福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集溜出物 |
| B、乙醇(乙醛):加新制Cu(OH)2溶液,加热至沸腾,过滤取溶液 |
| C、苯(苯酚):加NaOH溶液,充分振荡,分液,弃水层 |
| D、乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层 |
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高价氧化物的对应水化物是一种强酸;Z的非金属性在同周期主族元素中最强.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高价氧化物的对应水化物是一种强酸;Z的非金属性在同周期主族元素中最强. X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答: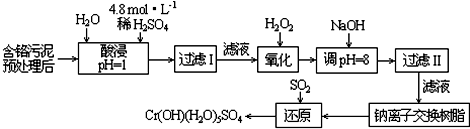

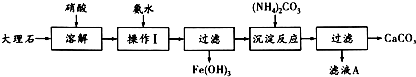
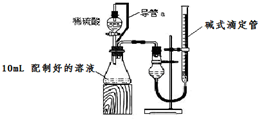 实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数w(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.
实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数w(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.