xR2++yH++O2=mR3++nH2O中,对m和R3+判断正确的是( )
| A、m=4,R3+是还原产物 |
| B、m=4,R3+是氧化产物 |
| C、2m=y,R3+是还原产物 |
| D、2m=y,R3+是氧化产物 |
下列反应属于氧化还原反应的是( )
| A、Fe(OH)3+3HCl=FeCl3+3H2O |
| B、FeCl3+3NaOH=Fe(OH)3↓+3NaCl |
| C、Na2O+CO2=Na2CO3 |
| D、Na2O2+SO2=Na2SO4 |
25℃时,10mL 0.1mol.L-1NH4Cl溶液中存在平衡:NH4++H2O?NH3?H2O+H+.对于该平衡,下列叙述正确的是( )
| A、加入大量水稀释时,平衡向右移动,溶液中c(H+)减小 |
| B、加入几滴浓盐酸,平衡向左移动,溶液的pH值增大 |
| C、加入几滴浓氨水,平衡向逆反应方向移动,c(OH-)减小 |
| D、升温至35℃,平衡向右移动,NH4Cl的水解程度减小 |
在5KCl+KClO3+3H2SO4═3Cl2↑+3K2SO4+3H2O中,被氧化与被还原的氯原子的物质的量比为( )
| A、5:1 | B、1:5 |
| C、1:1 | D、3:1 |
如图是某条件时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )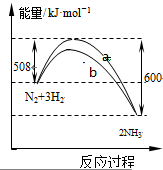

| A、加入催化剂可增大正反应速率,降低逆反应速率 |
| B、正反应的活化能大于逆反应的活化能 |
| C、b曲线是未加入催化剂时的能量变化曲线 |
| D、该反应的热化学方程式为:2NH3?N2+3H2△H=-92 kJ?mol-1 |
已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的( )
| A、X的能量一定高于M |
| B、因该反应为放热反应,故不必加热就可发生 |
| C、Y的能量一定高于N |
| D、X和Y的总能量一定高于M和N的总能量 |
有一无色混合物的水溶液,只能含有一下离子中的若干种;H+、K+、NH4+、Mg2+、Fe3+、Cl-、CO32-、SO42-,现取三份100ml溶液进行如下实验:根据上述实验,一下推测正确的是( )
(1)第一份加入足量AgNO3溶液有沉淀产生;
(2)第二份加入足量NaOH溶液加热后,收集到气体0.04mol;
(3)第三份加入足量BaCl2溶液后,得到沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
(1)第一份加入足量AgNO3溶液有沉淀产生;
(2)第二份加入足量NaOH溶液加热后,收集到气体0.04mol;
(3)第三份加入足量BaCl2溶液后,得到沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
| A、K+一定存在 |
| B、100ml溶液中含0.01molCO32- |
| C、Cl-一定存在 |
| D、Fe3+一定不存在,Mg2+可能存在 |
关于物质的变化、性质及用途,下列叙述中正确的是( )
| A、化学变化中有化学键的断裂与生成,并伴有能量的变化,物理变化二者都不具备 |
| B、简单非金属阴离子只有还原性,而简单金属阳离子只有氧化性 |
| C、工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏 |
| D、Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 |
下列事实不能用勒夏特列原理解释的是( )
| A、Fe(SCN)3溶液中存在Fe3++3SCN- Fe(SCN)3,向此溶液中加入固体KSCN后颜色变深 |
| B、用通过盛饱和食盐水的洗气瓶来除去氯气中的少量HCl气体杂质 |
| C、反应CO(g)+NO2(g)?CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
| D、合成氨:N2(g)+3H2(g)?2NH3 (g)△H<0在高温、高压和催化剂条件下进行 |