题目内容
xR2++yH++O2=mR3++nH2O中,对m和R3+判断正确的是( )
| A、m=4,R3+是还原产物 |
| B、m=4,R3+是氧化产物 |
| C、2m=y,R3+是还原产物 |
| D、2m=y,R3+是氧化产物 |
考点:氧化还原反应
专题:
分析:xR2++yH++O2═mR3++nH2O中,由原子守恒可知,x=m,n=2,y=4,由电荷守恒可知,2x+4=3m,所以m=4,该反应中R元素的化合价升高,O元素的化合价降低,以此来解答.
解答:
解:根据R原子守恒则x=m,根据电荷守恒则2x+y=3m,所以x=y=m,在反应中,R的化合价升高,所以R3+是氧化产物,氧元素化合价降低,所以H2O是还原产物.
A.m=4,R3+是氧化产物,故A错误;
B.m=4,R元素化合价升高,被 氧化,R3+是氧化产物,故正确;
C.m=4,y=4,则m=y,R3+是氧化产物,故C错误;
D.由以上分析可知m=y,故D错误.
故选B.
A.m=4,R3+是氧化产物,故A错误;
B.m=4,R元素化合价升高,被 氧化,R3+是氧化产物,故正确;
C.m=4,y=4,则m=y,R3+是氧化产物,故C错误;
D.由以上分析可知m=y,故D错误.
故选B.
点评:本题考查氧化还原反应,为高考常考考点,注意电荷守恒及原子守恒的应用,侧重基本概念的考查,明确反应中元素的化合价变化即可解答,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
下列各项叙述中,正确的是( )
| A、钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量 |
| B、价电子排布为4s24p3的元素位于第四周期第ⅢA族 |
| C、2p和3p轨道形状均为哑铃状,能量也相等 |
| D、在现代化学中,常利用原子光谱上的特征谱线来鉴定元素 |
Na2CO3俗名纯碱,下列对Na2CO3采用不同分类法的分类.不正确的是( )
| A、Na2CO3是碱 |
| B、Na2CO3是盐 |
| C、Na2CO3是正盐 |
| D、Na2CO3是钠盐 |
下列热化学方程式书写正确的是( )
A、2SO2+O2
| |||
| B、C(s)+O2(g)═CO2(g)△H=+393.5 kJ/mol | |||
C、500℃、30MPa下,将0.5mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)
| |||
| D、2.00gC2H2气体完全燃烧生成液态水和二氧化碳气体,放出99.6kJ的热量,该反应的热化学方程式为:2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2589.6kJ/moL |
如图是某条件时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )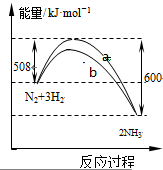

| A、加入催化剂可增大正反应速率,降低逆反应速率 |
| B、正反应的活化能大于逆反应的活化能 |
| C、b曲线是未加入催化剂时的能量变化曲线 |
| D、该反应的热化学方程式为:2NH3?N2+3H2△H=-92 kJ?mol-1 |
工业炼铁用到的原料有铁矿石、焦炭、空气、石灰石等,下列对原料在冶炼过程中的作用叙述不正确的是( )
| A、焦炭是铁矿石炼铁时的还原剂 |
| B、焦炭先与空气中的氧气反应,为炼铁提供能量 |
| C、石灰石是助矿石中杂质形成炉渣 |
| D、固体原料需粉碎,增大与气体的接触面 |
下列叙述中正确的是( )
| A、将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 |
| B、用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
| C、洗净的锥形瓶和滴定管可以放进烘箱中烘干 |
| D、氢氟酸试剂和NaOH溶液不可用带玻璃塞的玻璃瓶存放 |
从化学角度看,下列广告用语没有科学性错误的是( )
| A、金华米酒香甜可口,不含任何化学物质 |
| B、康师傅牌矿泉水,真正的纯水 |
| C、春晖牌蔬菜,天然种植,不含任何元素,真正的绿色食品 |
| D、云梦食用合格碘盐,可预防甲状腺肿大 |