用惰性电极电解含有0.400molCu(NO3)2和0.400mol KCl的混合溶液,一段时间后,在一个电极上析出0.300mol Cu,此时在另一电极上放出的气体在标准状况下的体积(标准状况下)为( )
| A、3.36L |
| B、6.72L |
| C、5.60L |
| D、2.80L |
下列说法正确的是( )
| A、金属晶体具有良好的延展性,是因为金属晶体中的原子层在滑动过程中金属键未破坏 |
| B、电子云图象中黑点的疏密是指电子数的多少 |
| C、含有极性键的分子一定是极性分子 |
| D、键能越大,表示该分子越容易受热分解 |
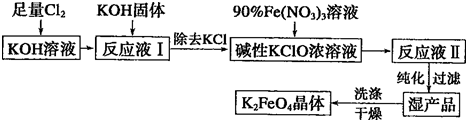

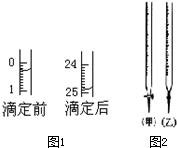 某研究性学习小组的同学用标准浓度的烧碱溶液测定未知浓度的盐酸.
某研究性学习小组的同学用标准浓度的烧碱溶液测定未知浓度的盐酸.