题目内容
下列是部分短周期中第二、第三周期元素的原子半径及主要化合价.
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族) .
(2)8个元素的最高价氧化物的水化物中,酸性最强的是 (填化学式).
(3)②元素和⑥元素形成的化合物的电子式是 .
(4)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式: .
(5)下列叙述正确的是 (填字母).
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
(1)⑧在元素周期表中的位置是(周期、族)
(2)8个元素的最高价氧化物的水化物中,酸性最强的是
(3)②元素和⑥元素形成的化合物的电子式是
(4)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:
(5)下列叙述正确的是
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:在第二、三周期元素中,主族元素的最高化合价与其族序数相等,故①③为第ⅠA族,⑤⑦为第ⅤA族,②⑨为第ⅡA族,同一主族元素,原子半径随着原子序数增大而增大,所以在①③中,①是Na元素,③是Li元素,在⑤⑦中,⑤是P元素,⑦是N元素,在②⑨中,、②是Mg元素,⑨是Be元素,④为第ⅢA族,半径小于镁元素大于铍元素,所以④是Al元素,⑥为第ⅤⅡA族,半径小于磷而大于氮,所以⑥是Cl元素,⑧为第ⅥA族,半径小于氮元素,所以⑧是O元素,故①是Na元素、②Mg元素、③是Li元素、④是Al元素、⑤是P元素、⑥是Cl元素、⑦是N元素、⑧是O元素,据此答题.
解答:
解:在第二、三周期元素中,主族元素的最高化合价与其族序数相等,故①③为第ⅠA族,⑤⑦为第ⅤA族,②⑨为第ⅡA族,同一主族元素,原子半径随着原子序数增大而增大,所以在①③中,①是Na元素,③是Li元素,在⑤⑦中,⑤是P元素,⑦是N元素,在②⑨中,、②是Mg元素,⑨是Be元素,④为第ⅢA族,半径小于镁元素大于铍元素,所以④是Al元素,⑥为第ⅤⅡA族,半径小于磷而大于氮,所以⑥是Cl元素,⑧为第ⅥA族,半径小于氮元素,所以⑧是O元素,故①是Na元素、②Mg元素、③是Li元素、④是Al元素、⑤是P元素、⑥是Cl元素、⑦是N元素、⑧是O元素,
(1)⑧是O元素,O原子核外有2个电子层,最外层有6个电子,所以在元素周期表中的位置是(周期、族)第二周期第ⅥA族,
故答案为:第二周期第ⅥA族;
(2)非金属的非金属性越强其最高价含氧酸的酸性越强,但氟元素没有含氧酸,所以非金属元素次之的是Cl元素,8个元素的最高价氧化物的水化物中,酸性最强的是HClO4,
故答案为:HClO4;
(3)②元素和⑥元素形成化合物是氯化镁,氯化镁的电子式是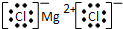 ,故答案为:
,故答案为: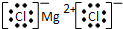 ;
;
(4)④最高价氧化物对应水化物是氢氧化铝,⑥的氢化物是盐酸,氢氧化铝和盐酸反应的离子方程式为:Al(OH)3+3H+=Al3++3H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;
(5)A.③是Li元素、④是Al元素,③、④处于不同周期,故正确;
B.②Mg元素,⑧是O元素,②的阳离子与⑧的阴离子的核外电子数相等,都是10个电子,故正确;
C.⑥是Cl元素,F在其同主族元素中非金属性最强,故错误;
D.⑤是P元素、⑦是N元素,二者位于同一主族,所以⑤元素与⑦元素两者核电荷数之差是8,故正确;
E.①是Na元素、⑧是O元素,①与⑧形成的化合物没有两性,故错误;
故选:ABD.
(1)⑧是O元素,O原子核外有2个电子层,最外层有6个电子,所以在元素周期表中的位置是(周期、族)第二周期第ⅥA族,
故答案为:第二周期第ⅥA族;
(2)非金属的非金属性越强其最高价含氧酸的酸性越强,但氟元素没有含氧酸,所以非金属元素次之的是Cl元素,8个元素的最高价氧化物的水化物中,酸性最强的是HClO4,
故答案为:HClO4;
(3)②元素和⑥元素形成化合物是氯化镁,氯化镁的电子式是
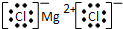 ,故答案为:
,故答案为: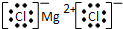 ;
;(4)④最高价氧化物对应水化物是氢氧化铝,⑥的氢化物是盐酸,氢氧化铝和盐酸反应的离子方程式为:Al(OH)3+3H+=Al3++3H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;
(5)A.③是Li元素、④是Al元素,③、④处于不同周期,故正确;
B.②Mg元素,⑧是O元素,②的阳离子与⑧的阴离子的核外电子数相等,都是10个电子,故正确;
C.⑥是Cl元素,F在其同主族元素中非金属性最强,故错误;
D.⑤是P元素、⑦是N元素,二者位于同一主族,所以⑤元素与⑦元素两者核电荷数之差是8,故正确;
E.①是Na元素、⑧是O元素,①与⑧形成的化合物没有两性,故错误;
故选:ABD.
点评:本题考查了原子结构和元素周期律的关系,正确推断元素是解本题关键,明确元素周期律的灵活运用,难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
下列表示物质结构的化学用语正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、NaCl的电子式: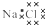 |
C、镁离子的结构示意图: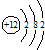 |
D、CH4的比例模型: |
在一定条件下,下列物质不能发生消去反应的是( )
| A、C2H5OH |
| B、(CH3)2CHCl |
| C、(CH3)3CCl |
| D、(CH3)3CCH2Cl |
大量事实证明,水溶液中并不存在H+、AlO2-等离子,实际存在的是H30+、[Al(OH)4]-.铝和强碱溶液的反应可以理解为铝在碱性环境下先与水反应,而后进一步与强碱反应(反应均不可逆).对于Al与重氢氧化钠(NaOD)的水溶液反应(假定水中不含氘和氚),下列说法正确的是( )
| A、生成的氢气中只含有D2 |
| B、生成的氢气中只含有H2 |
| C、生成的氢气中含有H2、HD、D2 |
| D、以上判断都不正确 |
如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )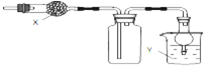

| A、X是碱石灰,收集到的气体是氯化氢,Y是水 |
| B、X是碱石灰,收集到的气体是氨气,Y是水 |
| C、X是氯化钙,搜集到的气体是二氧化硫,Y是氢氧化钠 |
| D、X是氯化钙,收集到的气体是一氧化氮,Y是氢氧化钠 |
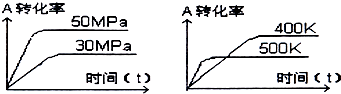 如图表示可逆反应mA(g)+nB(s)?xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是( )
如图表示可逆反应mA(g)+nB(s)?xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是( )| A、m>x,正反应为放热反应 |
| B、m+n<x,正反应为吸热反应 |
| C、m<x,正反应为放热反应 |
| D、m>x,正反应为吸热反应 |