将纯水加热至90℃时,下列叙述正确的是( )
| A、水的离子积变大、pH变小、呈酸性 |
| B、水的离子积不变、pH不变、呈中性 |
| C、水的离子积变小、pH变大、呈碱性 |
| D、水的离子积变大、pH变小、呈中性 |
氧化还原反应与四种基本反应类型的关系如图所示,则下列反应属于丙区域的是( )


| A、Cl2+2KBr═Br2+2KCl | ||||
B、2NaHCO3
| ||||
C、3Mg+N2
| ||||
| D、2Na2O2+2CO2═2Na2CO3+O2 |
根据下列三个反应的化学方程式:?I2+SO2+2H2O═H2SO4+2HI;2FeCl2+Cl2═2FeCl3,2FeCl3+2HI═2FeCl2+2HCl+I2有关物质的还原性依次增强的顺序是( )
?
?
| A、I->Fe2+>Cl->SO2 |
| B、Cl->Fe2+>SO2>I- |
| C、Fe2+>I->Cl->SO2 |
| D、SO2>I->Fe2+>Cl- |
已知如下氧化还原反应2BrO3-+Cl2=Br2+2ClO3- 5Cl2+I2+6H2O=2HIO3+10HCl ClO3-+5Cl-+6H+=3Cl2+3H2O
则下列各微粒氧化能力强弱顺序正确的是( )
则下列各微粒氧化能力强弱顺序正确的是( )
| A、ClO3->BrO3->IO3->Cl2 |
| B、BrO3->Cl2>ClO3->IO3- |
| C、BrO3->ClO3->Cl2>IO3- |
| D、Cl2>BrO3->ClO3->IO3- |
甲醇燃料电池(DMFC)可用于笔记本电脑、汽车、遥感通讯设备等,它的一极通入甲醇,一极通入氧气;电解质是质子交换膜,它能传导氢离子(H+).电池工作时,甲醇被氧化为二氧化碳和水,氧气在电极上的反应是O2+4H++4e-═2H2O.下列叙述中不正确的是( )
| A、负极的反应式为CH3OH+H2O-6e-═CO2↑+6H+ |
| B、电池的反应方程式是2CH3OH+3O2═2CO2+4H2O |
| C、电池工作时,H+由正极移向负极 |
| D、电池工作时,电子从通入甲醇的一极流出,经外电路再从通入氧气的一极流入 |
已知100mL0.55mol?L-1氢氧化钠溶液与100mL0.5mol?L-1盐酸溶液混合放出热量为a kJ(a>0).下列说法正确的是( )
| A、氢氧化钠和盐酸反应的中和热为a kJ |
| B、若其他条件不变,盐酸体积换成200 mL,则中和热为原来的2倍 |
| C、若其他条件不变,将氢氧化钠溶液换成200 mL,则放出热量2a kJ |
| D、若其他条件不变,将盐酸浓度换成0.55mol?L-1,则中和热不变 |
如图所示,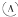 为直流电源,
为直流电源,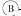 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路(未闭合K)后发现
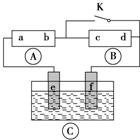
为电镀槽.接通电路(未闭合K)后发现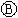 上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
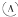 为直流电源,
为直流电源,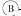 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路(未闭合K)后发现
为电镀槽.接通电路(未闭合K)后发现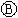 上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( ) 
| A、b为直流电源的负极 |
| B、f极为阴极,发生还原反应 |
| C、e极材料为铁片,f极材料的铜片 |
| D、可选用CuSO4溶液或CuCl2溶液作电镀液 |
将4mol SO2与2mol O2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2(g)+O2(g)?2SO3(g),测得平衡时SO3的浓度为0.5mol?L-1.则此条件下的平衡常数K( )
| A、4 | B、0.25 |
| C、0.4 | D、0.2 |
 如图为相互串联的甲、乙两电解池.试回答:
如图为相互串联的甲、乙两电解池.试回答: