题目内容
根据下列三个反应的化学方程式:?I2+SO2+2H2O═H2SO4+2HI;2FeCl2+Cl2═2FeCl3,2FeCl3+2HI═2FeCl2+2HCl+I2有关物质的还原性依次增强的顺序是( )
?
?
| A、I->Fe2+>Cl->SO2 |
| B、Cl->Fe2+>SO2>I- |
| C、Fe2+>I->Cl->SO2 |
| D、SO2>I->Fe2+>Cl- |
考点:氧化性、还原性强弱的比较
专题:
分析:同一自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,据此分析解答.
解答:
解:①I2+SO2+2H2O═2HI+H2SO4中还原剂是SO2、还原产物是HI,所以还原性SO2>HI;
②2FeCl2+Cl2═2FeCl3中还原剂是FeCl2、还原产物是FeCl3,所以还原性FeCl2>FeCl3;
③2FeCl3+2HI═I2+2FeCl2+2HCl中还原剂是KI、还原产物是FeCl2,所以还原性KI>FeCl2;
通过以上分析知,还原性强弱顺序是SO2>I->Fe2+>Cl-,
故选D.
②2FeCl2+Cl2═2FeCl3中还原剂是FeCl2、还原产物是FeCl3,所以还原性FeCl2>FeCl3;
③2FeCl3+2HI═I2+2FeCl2+2HCl中还原剂是KI、还原产物是FeCl2,所以还原性KI>FeCl2;
通过以上分析知,还原性强弱顺序是SO2>I->Fe2+>Cl-,
故选D.
点评:本题考查还原性强弱判断,侧重考查学生对基本概念的理解,根据元素化合价变化分析解答即可,知道常见元素化合价,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
鉴别某溶液中是含有Br-还是I-,可以选用的试剂是( )
| A、稀盐酸 | B、四氯化碳 |
| C、淀粉溶液 | D、四氯化碳和氯水 |
化学与资源、环境、生活关系密切,下列说法错误的是( )
| A、维生素C具有还原性,在人体内起抗氧化作用 |
| B、新型氢动力计程车可以降低PM2.5的排放,减少大气污染 |
| C、碘是人体必需微量元素,所以要多吃富含高碘酸的食物 |
| D、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱溶液会“断路” |
随着社会的发展,人们日益重视环境问题,下列做法或说法正确的是( )
| A、对农作物秸秆进行焚烧还田,以增加土壤肥力 |
| B、为提高农作物产量大量使用农药和化肥 |
| C、PM2.5是指大气中直径接近于2.5×10-6m(1m=109nm)的颗粒物,也称可吸入颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 |
| D、推广使用无磷洗衣粉,以减少水体富营养化 |
如图所示, 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路(未闭合K)后发现
为电镀槽.接通电路(未闭合K)后发现 上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
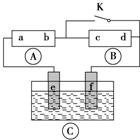
 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路(未闭合K)后发现
为电镀槽.接通电路(未闭合K)后发现 上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( ) 
| A、b为直流电源的负极 |
| B、f极为阴极,发生还原反应 |
| C、e极材料为铁片,f极材料的铜片 |
| D、可选用CuSO4溶液或CuCl2溶液作电镀液 |
下列实验过程中产生的现象与对应的图形相符的是( )
A、 NaHSO3 粉末加入HNO3溶液中 |
B、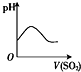 SO2气体通入新制氯水中 |
C、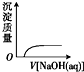 NaOH溶液滴入 Ba(HCO3)2溶液中 |
D、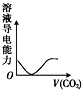 CO2气体通入澄清石灰水中 |
下列反应中必须加入还原剂才能进行的是( )
| A、FeCl3→FeCl2 |
| B、Zn→Zn2+ |
| C、H2→H2O |
| D、CuO→CuCl2 |
不需要其它试剂,只有几只试管和滴管而不能相互鉴别的物质组是( )
| A、氯化钡溶液和碳酸钠溶液 |
| B、氯化铝溶液和氢氧化钠溶液 |
| C、偏铝酸钠溶液和稀硫酸 |
| D、碳酸钠溶液和稀盐酸 |
下列离子方程式不正确的是( )
| A、向氢氧化钾溶液中滴加少量氯化铝溶液 Al3++4OH-=AlO2-+2H2O |
| B、在亚硫酸中加入过量的次氯酸钠溶液 H2SO3+3ClO-=Cl-+2HClO+SO42- |
| C、在稀HNO3溶液加入FeS固体 FeS+2H+=Fe2++H2S↑ |
| D、在过氧化钠中加入稀硫酸 2Na2O2+4H+=4Na++2H2O+O2↑ |