题目内容
将pH=1的盐酸平均分成两份,一份加入适量水,另一份加入于该盐酸物质的量浓度相同的适量NaOH溶液后,都升高可1,则加入的水与NaOH溶液的体积比为( )
| A、9 | B、10 | C、11 | D、12 |
考点:pH的简单计算
专题:电离平衡与溶液的pH专题
分析:常温下pH=1的盐酸中氢离子浓度为0.1mol/L,稀释后溶液的pH=2,氢离子浓度为0.01mol/L,稀释过程中盐酸的物质的量不变,据此计算出需要加入水的体积;
如果加入等浓度的氢氧化钠溶液,根据酸碱中和反应实质计算出需要加入氢氧化钠溶液的体积,然后计算出加入的水与NaOH溶液的体积比.
如果加入等浓度的氢氧化钠溶液,根据酸碱中和反应实质计算出需要加入氢氧化钠溶液的体积,然后计算出加入的水与NaOH溶液的体积比.
解答:
解:设每份盐酸的体积为VL,将pH=1的盐酸的物质的量浓度为0.1mol/L,加入水稀释后溶液的pH=2,稀释后溶液体积为10V,需要加入水的体积为9VL;
设加入0.1mol/L的NaOH溶液xL后溶液的pH变为2,则:
=0.01mol/L,解得:x=
V,
则加入的水与NaOH溶液的体积比为:9VL:
V=11,
故选C.
设加入0.1mol/L的NaOH溶液xL后溶液的pH变为2,则:
| 0.1mol/L×(V-x)L |
| (V+x)L |
| 9 |
| 11 |
则加入的水与NaOH溶液的体积比为:9VL:
| 9 |
| 11 |
故选C.
点评:本题考查了溶液pH的计算、物质的量浓度的计算,题目难度中等,试题侧重基础知识的考查,注意掌握溶液酸碱性与溶液pH的关系,明确物质的量浓度的概念及相关计算方法.

练习册系列答案
相关题目
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )


| A、1 mol A最多能与4 mol H2发生加成反应 |
| B、有机物A可以在一定条件下与HBr发生反应 |
| C、有机物A与浓硫酸混合加热,可以发生消去反应 |
| D、1 mol A与足量的NaOH溶液反应,最多可以消耗 2 mol NaOH |
甲醇燃料电池(DMFC)可用于笔记本电脑、汽车、遥感通讯设备等,它的一极通入甲醇,一极通入氧气;电解质是质子交换膜,它能传导氢离子(H+).电池工作时,甲醇被氧化为二氧化碳和水,氧气在电极上的反应是O2+4H++4e-═2H2O.下列叙述中不正确的是( )
| A、负极的反应式为CH3OH+H2O-6e-═CO2↑+6H+ |
| B、电池的反应方程式是2CH3OH+3O2═2CO2+4H2O |
| C、电池工作时,H+由正极移向负极 |
| D、电池工作时,电子从通入甲醇的一极流出,经外电路再从通入氧气的一极流入 |
在3NO2+H2O=2HNO3+NO↑反应中,氧化剂与还原剂的分子数之比为( )
| A、1:2 | B、2:1 |
| C、3:1 | D、1:3 |
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示.下列说法中正确的是( )
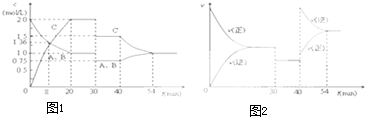

| A、第8min时 A的反应速率为0.08mol?L-1?min-1 |
| B、在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 |
| C、30min时改变的条件是降低温度,40min时改变的条件是升高温度 |
| D、反应方程式中的x=1,且正反应为放热反应 |
少量钠着火时,可用来灭火的物质或器材是( )
| A、煤油 | B、CO2 |
| C、砂土 | D、水 |
物质分类是化学研究的重要方法之一.化学工作者经常根据物质的组成对物质进行分类研究.近年来发现,在金星大气层中存在三氧化二碳.下列物质与它属于同类的是( )
| A、H2、O3 |
| B、H2SO4、H2CO3 |
| C、SO2、NO |
| D、Na2SO3、KClO3 |
 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;