1mol?L-1 H2SO4溶液的含义是( )
| A、1L水中含有1 mol H2SO4 |
| B、1L溶液中含1mol H+ |
| C、将98g H2SO4溶于1L水所配成的溶液 |
| D、指1L硫酸溶液中含有98g H2SO4 |
下列说法不正确的是( )
| A、18gH2O中所含电子数与NA个 NH4+所含电子数相同 |
| B、1 mol Na2O2固体中含离子总数为3NA |
| C、13g锌粒加入浓硫酸,反应后锌粒无剩余,得到标况下气体4.48L |
| D、将饱和食盐水加热蒸发少量水,冷却至原温度,溶液的质量分数增大 |
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
| A、25℃时,1 L pH=13的NaOH溶液中约含有6.02×1023个氢氧根离子 |
| B、1L 1 mol?L-1的盐酸中,所含氯化氢分子数为6.02×1023 |
| C、1 mol羟基(-OH)所含的电子数约为10×6.02×1023 |
| D、标准状况下,测得一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于6.02×1023 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、明矾溶液中K+和Al3+的物质的量浓度相等 |
| B、1mol 羟基和17g NH3所含的电子数相等 |
| C、常温常压下,l6gO2和16gO3中所含原子数均为NA |
| D、电解精炼铜时,外电路中转移电子数为2NA个时,阳极铜质量减少64g |
阿伏加德罗常数值记为NA,则关于C2H2(气)+O2(气)=2CO2(气)+H2O(液);H=-1300kJ/mol的下列说法中,正确的是( )
| A、有10NA个电子转移时,吸收1300kJ的能量 |
| B、有8NA个碳氧共用电子对生成时,放出1300kJ能量 |
| C、有NA个水分子生成且为液体时,吸收1300kJ能量 |
| D、有2NA个碳氧双键生成时,放出1300kJ能量 |
设NA为阿伏加德罗常数的值,下列说法中,正确的是( )
| A、2.4 g金属镁所含电子数目为0.2 NA |
| B、1 mol H2SO4所含粒子数目为NA |
| C、17 g NH3所含中子数目为10 NA |
| D、18 g水所含分子数目为NA |
己知:HCN(aq)与NaOH(aq)反应的△H=-12.1KJ/mol;HCl(aq)与NaOH(aq)反应的△H=-55.6KJ/mol.则HCN在水溶液中电离的△H等于( )
| A、-67.7 KJ/mol |
| B、-43.5 KJ/mol |
| C、+43.5 KJ/mol |
| D、+67.7 KJ/mol |
元素X、Y、Z原子序数之和为36,Y、Z在同一同期,X、Z在同一主族,X原子最外层电子数是Y原子最外层电子数的3倍.下列说法不正确的是( )
| A、同主族元素中X的气态氢化物沸点最高 |
| B、Z的氢化物与Z的最高价氧化物对应的水化物不能发生反应 |
| C、X、Y、Z三种元素可形成一种离子化合物 |
| D、X与Z所形成的化合物属于酸性氧化物 |
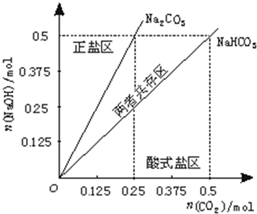 用NaOH、H2O、大理石和盐酸制取33g纯NaHCO3,请参照物质的溶解度回答下列问题:
用NaOH、H2O、大理石和盐酸制取33g纯NaHCO3,请参照物质的溶解度回答下列问题: