 如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )| A、1molH2中的化学键断裂时需要吸收436kJ能量 |
| B、2molHCl分子中的化学键形成时要释放862kJ能量 |
| C、稳定性:H2(g)>HCl(g) |
| D、此反应的热化学方程式为:H2(g)+Cl2(g)=2HCl(g)△H=-248kJ/mol |
实验表明,在一定条件下,乙烯和水反应可表示为:C2H4(g)+H2O(g)═C2H5OH(g)△H=-45.8kJ/mol
则下列说法中正确的是( )
则下列说法中正确的是( )
| A、实验中,乙烯的用量不会影响该反应的反应焓变△H |
| B、0.5molH2O(l)完全反应放出的热量为22.9kJ |
| C、1molC2H5OH(g)具有的能量大于1molC2H4(g)和1molH2O(g)所具有的能量和 |
| D、1molC2H4(g)和1molH2O (g)中化学键的总键能大于1molC2H5OH(g)中化学键的总键能 |
某反应的反应过程中能量变化如图所示,下列有关叙述不正确的是( )


| A、催化剂能改变反应的焓变 |
| B、催化剂能降低反应的活化能 |
| C、逆反应的活化能小于正反应的活化能 |
| D、催化剂可增大活化分子的百分数 |
 依据燃料电池的工作原理,设计如图所示的酒精检测仪,电池工作的原理是2CH3CH2OH+O2═2CH3CHO+2H2O,酒精蒸汽浓度越大,检测仪反映的电流越强.下列有关说法正确的是( )
依据燃料电池的工作原理,设计如图所示的酒精检测仪,电池工作的原理是2CH3CH2OH+O2═2CH3CHO+2H2O,酒精蒸汽浓度越大,检测仪反映的电流越强.下列有关说法正确的是( )| A、X极是正极,发生氧化反应 |
| B、电池工作时,H+向X极移动 |
| C、该条件下,检测结束后,Y极区pH增大 |
| D、电池工作时,毎转移4×10-3mol电子,消耗22.4ML氧气 |
对于锌-铜-稀H2SO4组成的原电池装置中,当导线中有1mol电子通过时,理论上的电极变化是( )
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了1gH2④铜片上析出1mol H2⑤溶液中的SO42-移向锌极⑥溶液中SO42-移向铜极.
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了1gH2④铜片上析出1mol H2⑤溶液中的SO42-移向锌极⑥溶液中SO42-移向铜极.
| A、①③⑤ | B、①④⑥ |
| C、②③⑤ | D、②④⑥ |
 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示,下列有关说法错误的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示,下列有关说法错误的是( )| A、电池反应为:2Al+3AgO+2NaOH═2NaAlO2+3Ag+H2O |
| B、当电极上析出1.08gAg时,电路中转移的电子为0.02mol |
| C、电子流动方向为:Al电极→电机→AgO/Ag电极→Al电极 |
| D、负极反应为Al-3e+4OH=AlO2+2H2O |
下列方法不能有效保护地下钢管的是( )
| A、涂上油漆 |
| B、与锌块相连 |
| C、与直流电源负极相连 |
| D、与直流电源正极相连 |
25℃、101kPa时,强酸与强碱的稀溶液发生中和反应的反应热又称为中和热(△H=-57.3mol?L-1),下列反应的反应热大于中和热的是( )
| A、H+(aq)+OH-(aq)=H2O(1)△H1 |
| B、Fe3+(aq)+3H2O(1)?Fe(OH)3(胶体)+3OH-(aq)△H2 |
| C、CH3COOH(aq)+OH-(aq)=CH3COO-(aq)+H2O(1)△H3 |
| D、2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(1)△H4 |
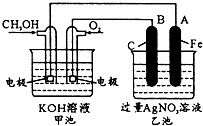 如图是一个化学过程的示意图.已知甲池的总反应式为:
如图是一个化学过程的示意图.已知甲池的总反应式为: