题目内容
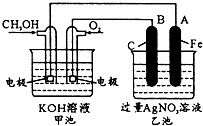 如图是一个化学过程的示意图.已知甲池的总反应式为:
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH
| 放电 |
| 充电 |
(1)请回答图中甲、乙两池的名称.甲电池是
(2)请回答下列电极的名称:通入CH3OH的电极名称是
(3)写出下列电极的电极反应式:通入O2的电极的电极反应式是
(4)乙池中反应的化学方程式为
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)甲装置中能自发的发生氧化还原反应是一个燃料电池;乙有外加电源,所以是电解池.
(2)根据得失电子判断正负极,根据外加电源判断阴阳极.
(3)氧气在正极上得电子;Fe为阴极,阴极上银离子得电子;
(4)依据电子守恒和电解的实质写出化学方程式;
(5)根据得失电子数相等找出银与氧气的关系式,然后计算.
(2)根据得失电子判断正负极,根据外加电源判断阴阳极.
(3)氧气在正极上得电子;Fe为阴极,阴极上银离子得电子;
(4)依据电子守恒和电解的实质写出化学方程式;
(5)根据得失电子数相等找出银与氧气的关系式,然后计算.
解答:
II.(1)甲装置中能自发的发生氧化还原反应是一个燃料电池,所以甲是把化学能转变为电能的装置,是原电池;乙有外加电源,所以是电解池;
故答案为:原电池;电解池;
(2)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以B石墨电极是阳极.
故答案为:负极;阳极;
(3)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 得电子和水反应生成氢氧根离子,发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极是阳极该电极上发生氧化反应,电极反应为:O2+2H2O+4e-=4OH-;铁电极是阴极,该电极上银离子得电子发生还原反应,电极反应为:4Ag++4e-=4Ag;
故答案为:O2+2H2O+4e-=4OH-;4Ag++4e-=4Ag;
(4)乙池中离子放电顺序为:阳离子 Ag+>H+,阴离子OH->NO3 -,阴极电极反应为:O2+2H2O+4e-=4OH-;阳极电极反应为:4Ag++4e-=4Ag;依据电子守恒和电解的实质写出化学方程式:4AgNO4+2H2O
4Ag+O2↑+4HNO3
故答案为:4AgNO4+2H2O
4Ag+O2↑+4HNO3;
(5)乙池中A(Fe)极是阴极,阴极的质量增加5.40g是银,其物质的量为
=0.05mol,
根据得失电子数相等,氧气与银的关系式为:
O2--------4Ag
22.4L 4mol
VL 0.05mol
则V=0.28L=280mL,
故答案为:280.
故答案为:原电池;电解池;
(2)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以B石墨电极是阳极.
故答案为:负极;阳极;
(3)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 得电子和水反应生成氢氧根离子,发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极是阳极该电极上发生氧化反应,电极反应为:O2+2H2O+4e-=4OH-;铁电极是阴极,该电极上银离子得电子发生还原反应,电极反应为:4Ag++4e-=4Ag;
故答案为:O2+2H2O+4e-=4OH-;4Ag++4e-=4Ag;
(4)乙池中离子放电顺序为:阳离子 Ag+>H+,阴离子OH->NO3 -,阴极电极反应为:O2+2H2O+4e-=4OH-;阳极电极反应为:4Ag++4e-=4Ag;依据电子守恒和电解的实质写出化学方程式:4AgNO4+2H2O
| ||
故答案为:4AgNO4+2H2O
| ||
(5)乙池中A(Fe)极是阴极,阴极的质量增加5.40g是银,其物质的量为
| 5.4g |
| 108g/mol |
根据得失电子数相等,氧气与银的关系式为:
O2--------4Ag
22.4L 4mol
VL 0.05mol
则V=0.28L=280mL,
故答案为:280.
点评:本题考查了原电池和电解池的工作原理的应用,主要考查了是电池判断、电极判断,电解方程式的书写、电子守恒的应用等,题目难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
常温下单质硫主要以S8形式存在,加热时,S8会转化为S6、S4、S2等.当温度达到750℃时,硫蒸汽主要以S2形式存在(占92%).下列说法正确的是( )
| A、不论哪种硫分子,完全燃烧时都生成SO2 |
| B、把硫单质在空气中加热到750℃即得S2 |
| C、常温条件下单质硫为原子晶体 |
| D、S8转化为S2、S4、S6属于物理变化 |
以色列科学家发现准晶体独享2011年诺贝尔化学奖,已知的准晶体都是金属互化物.有关准晶体的组成与结构的规律仍在研究之中,人们发现组成为铝-钢-铁-铬的准晶体具有低摩擦系数、高硬度、低表面能以及低传热性,正被开发为炒菜锅的镀层.下列说法正确的是( )
| A、准晶体可开发成为新型材料 |
| B、准晶体不能作耐高温材料 |
| C、准晶体是共价化合物 |
| D、在电镀池中用铁锅作阳极时可以在表面镀上准晶体镀层 |
反应2SO2+O2?2SO3经一段时间后,SO2的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L?s).则这段时间为( )
| A、0.1s | B、2.5s |
| C、5s | D、10s |
 依据燃料电池的工作原理,设计如图所示的酒精检测仪,电池工作的原理是2CH3CH2OH+O2═2CH3CHO+2H2O,酒精蒸汽浓度越大,检测仪反映的电流越强.下列有关说法正确的是( )
依据燃料电池的工作原理,设计如图所示的酒精检测仪,电池工作的原理是2CH3CH2OH+O2═2CH3CHO+2H2O,酒精蒸汽浓度越大,检测仪反映的电流越强.下列有关说法正确的是( )| A、X极是正极,发生氧化反应 |
| B、电池工作时,H+向X极移动 |
| C、该条件下,检测结束后,Y极区pH增大 |
| D、电池工作时,毎转移4×10-3mol电子,消耗22.4ML氧气 |
由M层有2个电子的元素X与L层有5个电子的元素Y形成的化合物的化学式为( )
| A、XY |
| B、X2Y3 |
| C、X3Y2 |
| D、X2Y5 |