设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、35.5g超氧化钾(KO2)所含的阴离子中电子数为8NA |
| B、标准状况下,11.2L氯仿中含有的C-Cl键的数目为1.5NA |
| C、常温常压下,92g NO2和N2O4混合气体中含有的原子数为6NA |
| D、工业上铜的电解精炼时电解池中每转移1mol电子时阳极上溶解的铜原子数为0.5NA |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA |
| B、1mol H2O2完全分解生成H2O和O2时,转移了NA个电子 |
| C、1mol C10H22分子中,含有共价键数目为32NA |
| D、0.5mol Na2O2中含有NA个阴离子 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,11.2L乙烯中含有的原子数为2NA |
| B、1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
| C、标准状况下,44.8LNO与22.4LO2混合后的气体中含有的分子数为3NA |
| D、常温下,1L0.1mol?L-1 NH4NO3溶液中含有的NH4+和NO3-的总数为0.2NA |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、58.5g氯化钠中约含有6.02×1023个氯化钠分子 |
| B、含有2NA个阴离子的CaC2,在标准状况下,能产生约44.8L的乙炔气体 |
| C、在含4mol Si-O键的石英晶体中,氧原子的数目为4NA |
| D、12.5mL 16mol?L-1浓硫酸与足量锌反应,转移电子数为0.2NA |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| B、标准状况下,22.4L己烷中共价键数目为19NA |
| C、由SO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| D、1L浓度为1mol?L-1的Na2CO3溶液中含有NA个CO32- |
阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是( )
| A、2.4g 镁作还原剂时失去电子数是0.1×6.02×1023 |
| B、标准状况下,22.4L 氮气中含有的共价键数是6.02×1023 |
| C、标准状况下,5.6 L的甲醛所含的电子数是4×6.02×1023 |
| D、100mL 1mol/L氨水溶液中,铵根离子的个数0.1×6.02×1023 |
有关下列说法正确的是( )
| A、6.8g熔融KHSO4与3.9g Na202阴离子数目相同 |
B、某金属阳离子的结构为: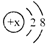 与Cl-形成的强电解质都是离子化合物 与Cl-形成的强电解质都是离子化合物 |
C、二硫化碳是直线型的分子,其电子式是: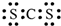 |
| D、因为氯、溴、碘非金属性逐渐减弱,所以其氢化物酸性HCl>HBr>HI |
下列说法中正确的是( )
| A、非金属原子组成的化合物不可能是离子化合物 |
| B、ⅠA族元素的金属性一定比ⅡA族元素的金属性强 |
| C、同一主族元素组成的化合物一定是共价化合物 |
| D、NH4H中的所有原子的最外层都符合相应稀有气体原子电子层结构,1mol NH5中含有4NA个N-H键(NA表示阿伏加德罗常数的值) |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,1mol乙烯共用电子对数为4NA |
| B、1mol乙醛与足量新制Cu(OH)2悬浊液反应,转移电子数目为NA |
| C、标准状况下,1L戊烷充分燃烧后生成气态产物的分子数为5/22.4 NA |
| D、0.1mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6 NA |
等质量的下列物质与足量稀盐酸反应,产生气体质量最大的是( )
| A、Na |
| B、Na2O2 |
| C、Na2CO3 |
| D、NaHCO3 |